|
ბრუგადას სინდრომი
ტ.
ნამორაძე საკვანძო სიტყვები: უეცარი გულისმიერი სიკვდილი, ელექტროკარდიოგრაფია, ბრუგადას სინდრომი. |
|
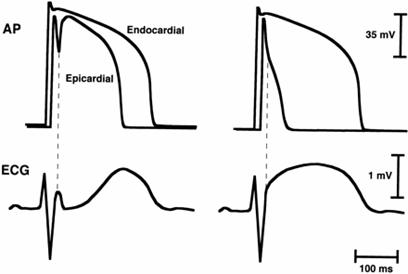
1992 წელს ძმებმა პედრო და ხოზეფ ბრუგადეებმა გამოაქვეყნეს სტატია სათაურით “ჰისის კონის მარჯვენა ფეხის ბლოკადა, შთ სეგმენტის მყარი ელევაცია და უეცარი გულისმიერი სიკვდილი: განსხვავებული კლინიკური და ელექტროკარდიოგრაფიული სინდრომი. მულტიცენტრული გამოკვლევა”[1] სადაც აღწერეს ადრე წარმოებული დაკვირვება რვა პაციენტზე. ყველა შემთხვევაში ადგილი ჰქონდა მორეციდივე, სწრაფად კუპირებადი უეცარი სიკვდილის ეპიზოდებს. მკვლევარებმა ეს პაციენტები გამოყვეს პარკუჭოვანი არიტმიით დაავადებულთა იმ ჯგუფიდან, რომელთაც არ ჰქონდათ გულის სტრუქტურული დაზიანება. ყველა ავადმყოფის (6 მამაკაცი, 2 ქალი) კლინიკური და ელექტროკარდიოგრაფიული (ეკგ) მონაცემები განსხვავდებოდა პაციენტებისაგან, რომელთაც აღენიშნებოდათ იდიოპათიური პარკუჭოვანი ფიბრილაცია. პაციენტებს ჩაუტარდათ ეკგ, ექოსკოპიური, ელექტროფიზიოლოგიური, ანგიოგრაფიული, ჰისტოლოგიური გამოკვლევები, ფიზიკური დატვირთვის ცდა. ეკგ-ზე სინუსური რიტმის პირობებში, ადგილი ჰქონდა ჰისის კონის მარჯვენა ფეხის ბლოკადას, ST სეგმენტის მყარ ელევაციას მარჯვენა პრეკორდიალურ – V1V2V3 განხრებში, ნორმალურ QT ინტერვალს. აღნიშნული ცვლილებები არ აიხსნებოდა გულის იშემიით, სტრუქტურული დარღვევებით ან ელექტროლიტური დისბალანსით. ოთხ პაციენტს ჩაუტარდა პარკუჭის ბიოფსია, სადაც ჰისტოლოგიურ გადახრები არ აღინიშნა. სწრაფად კუპირებადი, უეცარი სიკვდილის ეპიზოდები დაკავშირებული იყო პოლიმორფულ პარკუჭოვან ტაქიკარდიასთან, რომელიც იწყებოდა პარკუჭოვანი ბიგემინური ექსტრასისტოლებით. პროგრამული ელექტროსტიმულაციით მსგავსი არიტმია შვიდიდან ოთხ შემთხვევაში იქნა მიღებული. გამოკვლეულთაგან ოთხს ჩაედგა იმპლანტირებული კარდიოვერტდეფიბრილატორი, დანარჩენებს დემანდ ტიპის პარკუჭოვანი რიტმის მატარებელი. ავტორები მივიდნენ დასკვნამდე, რომ შესწავლილ პაციენტთა მსგავსი კლინიკური და ეკგ მონაცემები არის განსხვავებული სინდრომი, რომლის მიზეზი უცნობია. შემდგომში აღნიშნული სინდრომს უწოდეს ბრუგარდას სინდრომი [2,3] და დაიწყო მისი ინტენსიური კვლევა მსოფლიოს მრავალ ქვეყანაში. ბრუგადას სინდრომი განიმარტება, როგორც არიტმოგენული, ოჯახური აუტოსომურ-დომინანტური ტიპის დაავადება, გამოვლენილი სინკოპეთი, უეცარი, გარდამავალი სიკვდილის ეპიზოდებით, ეკგ-ზე V1V2V3 განხრებში შთ სეგმენტის დამახასიათებელი ელევაციით, გამოწვეული SCN5A გენის მუტაციით, რომელიც კარდიომიოციტის მემბრანის ნატრიუმის არხს აკოდირებს. პარკუჭოვანი ტაქიარითმია და ფიბრილაცია უეცარი სიკვდილის მიზეზი ხდება. 1989 წელს Martini. et. al [4] მიერ აღწერილი ექვსი პაციენტის ეკგ და მიმდინარეობა პარკუჭოვანი ფიბრილაციის სახით წააგავდა ბრუგადას სინდრომს, მაგრამ განსხვავდებოდა გულის სტრუქტურული დაზიანების არსებობით. 2005 წელს ჩატარებულ ბრუგადას სინდრომის კონსენსუს კონფერენციაზე [5] აღინიშნა, რომ ბრუგადას სინდრომის სიხშირე, რომელიც იშვიათ დაავადებად ითვლებოდა, ამჟამად ზოგიერთ ქვეყანაში ახალგაზრდა პირებში, სიკვდილიანობის შემთხვევებით მხოლოდ ავტოავარიებში დაღუპული ადამიანების რაოდენობას ჩამორჩება. უეცარი სიკვდილის შემთხვევების ყველაზე ხშირ მიზეზად გულის იშემიური დაავადება 80-85%, კარდიომიოპათიები 10-15% მიიჩნება [6,7] დანარჩენს 5-10% არის იდიოპათიური პარკუჭოვანი ტაქიკარდია, ბრუგადას სინდრომი, გახანგრძლივებული QT და სხვა. ზოგიერთი მონაცემით [8,9] ბრუგადას სინდრომის მიზეზით სიკვდილიანობა 4-12%, ხოლო სტრუქტურულად ნორმალური გულით დაღუპულთაგან 20%-ია. გავრცელების სიხშირე ენდემურ რეგიონებში-სამხრეთ აზიის ზოგიერთ ქვეყანაში 0,05-0,66% აღწევს. ამ ქვეყნებში ღამის საათებში უეცარი სიკვდილის შემთხვევები იმდენად ხშირია, რომ მას თავისი სახელწოდებებიც კი აქვს: ტაილანდში-Lai Tai (სიკვდილი ძილში), იაპონიაში-Pokkuri- (უეცარი მოულოდნელი სიკვდილი ღამით), ხოლო ფილიპინებზე-Bangungut (კვნესა და სიკვდილი ძილში). ჩვენში ამას “ძილში გაპარვას” უწოდებენ. ბუნებრივია, ეს ხშირად გულის ორგანული დაავადებების ფონზე ვითარდება. ზოგიერთი გამოკვლევით Lai tai დაკავშირებულია ამ პოპულაციაში ენდემურ თირკმლის დისტალურ ტუბულარულ აციდოზთან, ჰიპოკალიემიურ პერიოდულ დამბლასთან და თირკმელკენჭოვან დაავადებასთან [10]. იაპონიაში კი Pოკკური-ს დროს გარდაცვლილთა გულის გამტარებელ სისტემაში ხშირად შეფერხებებს ჰქონდა ადგილი[11]. თუმცა ბოლო დროს, ბრუგადას სინდრომის აღმოჩენის შემდეგ, იგივე ქვეყანაში ამ სინდრომის დიდი სიხშირე დადგინდა [12]. იაპონიაში ბრუგადას ტიპის ეკგ-ს სიხშირემ 0,7% შეადგინა, ცალკე მამაკაცებში კი 2,14% [13]. სხვა მონაცემებით ბრუგადას ტიპის ეკგ 0,16%-ში დადგინდა [14]. იაპონიაში უეცარი გულისმიერი სიკვდილით დაღუპულთა შორის ბრუგადას ტიპის ეკგ 26% აღინიშნა [15]. ფინეთში ჩატარებულ გამოკვლევით ბრუგადას I ტიპის ეკგ არ დაფიქსირდა, II და III ტიპის ეკგ სიხშირე 0,55-0,61%-ს შეადგენდა [16]. ეკგ ტიპებზე დაწვრილებით ქვევით გვექნება საუბარი. რუსული სამედიცინო ჟურნალებიდან ვნახეთ ორი შემთხვევის აღწერა [17,18] და ერთი ლიტერატურის მიმოხილვა [19]. ეტიოლოგია და პათოგენეზი: ამჟამად დაგროვდა ბევრი მონაცემი ბრუგადას სინდრომის გენეტიკური ბუნების შესახებ. გენეტიკური ანალიზის ჩატარება საბოლოო დიაგნოზის დასადგენად მეტად სასარგებლო უნდა იყოს, თუმცა ამისთვის გარკვეული შეზღუდვები არსებობს. როგორც მიუთითებენ [9] SCN5A გენის მუტაციის იდენტიფიკაციას, რომელიც ბრუგადას სინდრომთანაა დაკავშირებული, კვირეები და ზოგჯერ თვეებიც სჭირდება, ცოტაა დიაგნოსტიკური ლაბორატორიები, რომლებსაც დაავადების სკრინინგის ჩატარება შეუძლიათ, წარმატებული გენოტიპირება შესაძლებელია ავადმყოფთა მხოლოდ 20-30% და ბოლოს, სპორადიულ შემთხვევებში საეჭვოა მუტაციების დადგენა. მიუხედავად ამისა გენეტიკური ანალიზი სულ უფრო ფართოდ ინერგება და ბევრ სასარგებლო ინფორმაციას იძლევა. ცნობილია, რომ ბრუგადას სინდრომის 3p21-24 ქრომოსომის SCN5A გენთან დაკავშირება პირველად 1998 წელს მოხდა [20]. ავტორებმა დაადგინეს, რომ SCN5A გენის მუტაციის პირობებში სწრაფად ხდება ნატრიუმის არხის ინაქტივაცია და შემდგომში ფუნქციის დაკარგვა. ისინი ამ დასკვნამდე მივიდნენ იდიოპათიური პარკუჭოვანი არითმიის ჯგუფიდან განსხვავებული ეკგ მონაცემებით გამოყოფილი სამი ოჯახის გენეტიკური ანალიზის ჩატარების შედეგად. აღნიშნული გენით კოდირდება მიოფიბრილების მემბრანის ნატრიუმის არხების ალფა-ქვეერთეული. გენის მუტაცია იწვევს ნატრიუმის არხების უკმარისობას, ნატრიუმის დენის შემცირებას, ვოლტაჟის გრადიენტს და დროის შემოკლებას [21,22,23]. მიუთითებენ, რომ არხების ინაქტივაცია ხდება არა ოთახის არამედ სხეულის ტემპერატურაზე [24], რის გამოც ცხელების დროს არიტმიის დაწყების რისკი მატულობს. ამჟამად, მემბრანის არხების პათოლოგიას დიდი როლი ენიჭება, როგორც გულსისხლძარღვთა ისე სხვა სისტემების დაავადებების დროსაც, როგორიცაა შაქრიანი დიაბეტი, მიოტონია, ეპილეფსია. გამოყოფილია შესაბამისი გენები [25], რომელთა მუტაციები აღნიშნულ დაავადებებს იწვევს სწორედ მემბრანების ცილოვანი არხების პათოლოგიის გამო. მეორე მხრივ დადგინდა, რომ SCN5A გენის მუტაცია კავშირშია არა მარტო ბრუგადას სინდრომთან, არამედ ლენეგრეს დაავადებასთანაც (გამტარებელი სისტემის პროგრესული მემკვიდრული დაავადება). ლენეგრეს დაავადების მოდელად გამოიყენეს SCN5A +/- რიგის ჰეტეროზიგოტური თაგვები. მიიჩნევენ, რომ ლენგრეს დაავადების ფენოტიპი, რომელიც მოიცავს ასაკთან დაკავშირებულ პროგრესულ დაავადებას გამტარებელ სისტემაში, დაკავშირებულია მიოკარდიუმის ფიბროზთან. [26]. ამავე საკითხთანაა დაკავშირებული. კლინიკური და გენეტიკური გამოკვლევა ოჯახის წევრების, სადაც SCN5A გენის მუტაციების 13 შემთხვევიდან ხუთ პიროვნებას ბრუგადას სინდრომი აღენიშნება, ხოლო რვას გამტარებლობის იზოლირებული დეფექტი [27]. SCN5A გენის მუტაცია უფრო ხშირად დაკავშირებულია ბრუგადას სინდრომის ფენოტიპთან მამაკაცებში და გამტარებელ სისტემის დაავადების ფენოტოპთან ქალებში, რის შესახებაც არსებობს ექსპერიმენტული მონაცემებიც [28]. დამტკიცებულია, რომ სხვადასხვა გენების მუტაცია იწვევს არხების პათოლოგიას და ხდება რიგი არიტმიების საფუძველი როგორიცაა გახან-გრძლივებული Qთ სინდრომის ყველა ფორმა- რომანოვარდის, ჯერველ-ლანგ ნილსენის, ანდერსენის, აგრეთვე ბრუგადას სინდრომი, იდიოპათიური პარკუჭოვანი ფიბრილაცია, კატექოლამინერგული პარკუჭოვანი ტაქიკარდია, სინუსის კვანძის სისუსტე, ოჯახური-მოციმციმე არითმია, მოკლე Qთ სინდრომი [29,30], აგრეთვე დილატაციური და ჰიპერტროფიული კარდიომიოპათია. [31,32]. დავუბრუნდეთ კვლავ SCN5A გენს, მისი მუტაცია დაკავშირებულია აგრეთვე მე-3 ტიპის გახანგრძლივებულ QT გენს, მისი მუტაცია დაკავშირებულია აგრეთვე მე-3 ტიპის (გახანგრძლივებულ QT3 სინდრომთან. [33,34]. განსხვავებით ბრუგადას სინდრომისაგან, ადგილი აქვს Nა-ის არხის ფუნქციის გაძლიერებას [35]. ამასთან თუ გახანგრძლივებული QT და გამტარებლობის დარღვევა დაბადებისთანავე გამოისახება ეკგ-ზე, შთ სეგმენტის ელევაცია, 5 წლის ასაკის შემდეგ ყალიბდება [36]. ბრუგადას სინდრომის შემთხვევაში ავადმყოფებს, რომელთაც SCN5A გენის განსხვავებული ლოაკუსი აქვთ მე-3 ქრომოსამაში- 3p22-25- აღენიშნებათ პროკაინამიდის ტესტის მიმართ დაბალი მგრძნობელობა, გამტარებლობის პროგრესული დარღვევა და შედარებით უკეთესი პროგნოზი. [37]. ავტორთა მიერ აღწერილ ფორმას ბრუგადას სინდრომი-2 უწოდეს [30]. SCN5A გენის მუტაციამ შეიძლება გამოიწვიოს იდიოპათიური პარკუჭოვანი ფიბრილაციოს შეტევები ტიპიური ბრუგადას ეკგ ცლილებების გარეშეც [38] ხოლო Hong et el [39] თვლიან, რომ უეცარი აუხსნელი სიკვდილის სინდრომი და ბრუგადას სინდრომი ერთიდა იგივე დაავადებაა. ბრუგადას ტიპის ეკგ ფორმირების ელექტროფიზიოლოგიური მექანიზმები შემდეგნაირადაა წარმოდგენილი. ნორმალურ პირობებში ST სეგმენტი იზოელექტრულ ხაზზეა, რადგან არაა ვოლტაჟის ტრანსმურალური გრადიენტი მოქმედების პოტენციალის პლატის დონეზე. როგორც მიუთითებენ [40,41] მოქმედების პოტენციალის ჰეტეროგენობა ქმნის ვოლტაჟის ტრანსმურალურ გრადიენტს და საფუძველს აძლევს ელექტროკარდიოგრამაზე J (ოსბორნის) კბილის გამოჩენას. როცა J წერტილი ანუ QRS-is ST- სთან შერწყმის წერტილი იზოხაზიდან ძლიერადაა გადახრილი მას J გადახრას ანუ J კბილს, გვიან დელტა კბილს უწოდებენ [42] ანუ ესაა პატარა მეორადი r კბილი (r’) – Rკბილს დაღმავალი ტოტის დაკბილვა [2,42]. J კბილის გაჩენას უკავშირებდნენ სხეულის ტემპერატურის დაქვეითებას, ჰიპერკალციემიას, სუბარაქნოიდურ სისხლჩაქცევას და ა.შ. როგორც, აღინიშნა ტრანსმურალური გრადიენტის გაჩენა იწვევს J კბილს და ST სეგმენტის ელევაციას, რაც ჩანს სურ #1-ზე.
სურათი #1 ეპიკარდიული და ენდოკარდიული მოქმედების პოტენციალთა შორის სხვაობის გამოსახულება [44]. მოყვანილია [2,45] მიხედვით. ზედა სტრიქონზე ეპიკარდიული და ენდოკარდიული მოქმედების პოტენციალებია (AP), ქვედაზე-სხეულის ზედაპირიდან ჩაწერილი ეკგ. ზედა მარცხენა გამოსახულებაზე ჩანს ეპიკარდიული მოქმედების პოტენციალის I ფაზის წინ წარზიდული დაკბილვა, რაც შეესაბამება J კბილს ეკგ-ზე. ზედა მარჯვენა გამოსახულებაზე ეპიკარდიული მოქმედების პოტენციალის თაღის დაკარგვა ამცირებს მოქმედების პოტენციალის ხანგრძლივობას, რაც იწვევს ტრანსმურალურ ჰეტეროგენობას და ST სეგმენტის ელევაციას ეკგ-ზე- გამოსახულება ქვევით მარჯვნივ. ექსპერიმენტში ST ელევაცია და J კბილი იძლევა R’ კბილის, რაც სავარაუდოს ხდის არა გამტარებლობის ბლოკადას ჰისის კონის მარჯვენა ფეხში, არამედ მარჯვენა პარკუჭის ეპიკარდიუმის სწრაფ რეპოლარიზაციას. ამიტომ მარჯვენა ფეხის ბლოკადას დიაგნოზის დასადგენად მისი ყველა მკაცრი კრიტერიუმი უნდა განიხილებოდეს [8]. კონტაქტურ-ელექტროდული მეთოდით ღია გულმკერდის პირობებში Kurita et al [46] უშუალოდ შეისწავლეს ST სეგმენტის ელევაციის ელექტროფიზიოლოგიური მექანიზმი ბრუგადას სინდრომის დროს. მარჯვენა პარკუჭის გამოსასვლელი ტრაქტის ეპიკარდიუმიდან ჩაწერილი მონოფაზური მოქმედების პოტენციალის მრუდზე, განსხვავებით ენდოკარდიუმიდან ჩაწერილი მრუდისგან აღინიშნება მოქმედების პოტენციალის მრუდის ამოზნექილი დაკბილვა პიკი და თაღის (Spike and Dome) კონფიგურაციით, რაც ადასტურებს ზევით აღწერილ ექსპერიმენტულ მონაცემებს, სურ #1-ზე. რეპოლარიზაციის ჰეტეროგენული ტრანსმურალური დისპერსია, რომელიც ექსპერიმენტში ნატრიუმის არხის ბლოკატორ ფლეკაინიდით და აცეტილქოლინით შთ ელევაციას იწვევს, საფუძველია მე-2 ფაზის რეენტრული ექსტრასისტოლის, რაც შემდგომში პარკუჭოვანი ტაქიკარდიის და ფიბრილაციის მიზეზი ხდება [40]. ამავე ექსპერიმენტით დამტკიცდა, რომ ქინიდინს და 4-ამინოპირიდინს შეუძლიათ ST სეგმენტის ნორმალიზაცია და პარკუჭოვანი არითმიების პრევენცია.
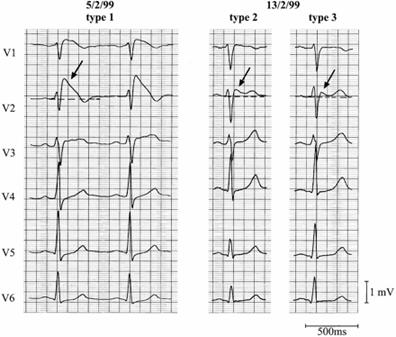
განსხვავებული ელექტროფიზიოლოგიური მექანიზმები საფუძვლად უდევს ადრეული რეპოლარიზაციის სინდრომს, გახანგრძლივებულ Qთ სინდრომს და ბრუგადას სინდრომს, რაც ნათლად ჩანს მოქმედების პოტენციალის მრუდებით სურ #2-ზე. სურათი #2 ელექტროფიზიოლოგიური განსხვავევები ადრეული რეპოლარიზაციის სინდრომს, გახანგრძლივებულ QT სინდრომს და ბრუგადას სინდრომს შორის.[47] პირველ შემთხვევაში ვოლტაჟის გრადიენტი ST ეელევაციას იძლევა, მაგრამ მოქმედების პოტენციალის ხანგრძლივობის დისპერსიას ადგილი არა აქვს რის გამოც არიტმიები არ ვითარდება. მეორე შემთხვევაში, ხანგრძლივი QT სინდრომის დროს არის ვოლტაჟის გრადინტი ზოგიერთ უბანში მოქმედების პოტენციალის გახანგრძლივების გამო ადრეული შემდგომი დეპოლარიზაციის საფუძველზე. ვოლტაჟის გრადიენტი მე-2 ფაზის რეენტრის იძლევა და ბოლოს ბრუგადის სინდრომის დროს რეენტრი ვითარდება მოქმედების პოტენციალის შემოკლების გამო (მე-3 გამოსახულება). რეენტრით გამოწვეული ადრეული პარკუჭოვანი შეკუმშვები პარკუჭოვანი ფიბრილაციის 23 ეპიზოდის წინ 22 შემთხვევაში დააფიქსირეს [48], რაც მათ “გამშვებ” როლზე მიუთითებს. ფლეკაინიდით ინდუცირებული ბრუგადას ტიპის ეკგ-ს გაჩენისას გამოჩნდა კუმშვადობის დაწყების შეფერხება მარჯვენა და მარცხენა პარკუჭებს შორის, მარჯვენა პარკუჭის განდევნის ფაზის ხანგრძლივობის შემოკლება, რაც კორელირებდა შთ სეგმენტის აწევის სიდიდესთან [49]. ავტორები თვლიან, რომ აღნიშნული მექანიზმი გამოწვეული გამტარებლობის შეფერხებით, ისევე როგორც მექანიზმი მარჯვენა პარკუჭის სუბეპიკარდიული პოტენციალის სელექტიური შემოკლების, მხედველობაში უნდა იყოს მიღებული. მიუთითებენ პარასიმპატიკური გავლენის შესახებ ბრუგადას სინდრომის დროს [50]. აუტონომიური რეეულაციის როლის დასადგენად გამოიყენეს პოზიტრონული ემისიური ტომოგრაფიის მეთოდი ნორადრენალინის ანალოგის [123] m-იოდბენზილგუანიდინის მოხმარების მიხედვით [51]. იზოტოპის ავსების დაქვეითებამ დაადასტურა სიმპატიკური პრესინაფსური დისფუნქცია. ბრუგადას სინდრომის დროს უეცარი სიკვდილი ან პარკუჭოვანი არითმიები ვითარდება მოსვენებისას ან ძილში, რაც საფიქრებელს ხდის პარასიმპატიკურ ზემოქმედებას, როგორც გამშვებ ფაქტორს. ST სეგმენტის ელევაცია მატულობს b-ბლოკადით ან პარასიმპატიკური სტიმულაციით, ხოლო კლებულობს ან ქრება b-სტიმულაციით [52,53]. ST სეგმენტის ელევაციაზე და პარკუჭოვანი ფიბრილაციის აღმოცენებაზე ვაგუსური გაღიზიანება აცეტილქოლინის და ერგონავინ მალეატის საშუალებით კორონაროგრაფიის დროს დაადასტურეს Noda et al [54]. ავტორები თვლიან, რომ როგორც ვაგუსური გაღიზიანება ისე მსუბუქი იშემია ბრუგადას სინდრომის შემთხვევაში აძლიერებს ST სეგმენტის ელევაციის და პარკუჭოვანი ფიბრილაციის განვითარების შესაძლებლობას. ჰოლტერის მონიტორირების დროს ღამის საათებში 5 წუთიანი საშუალო N-N ინტერვალის სტანდარტული გადახრის მნიშვნელოვანი შემცირება აღინიშნა სიმპტომურ პაციენტებში უსიმპტომო პაციენტებთან შედარებით [55]. (N-N ინტერვალი ანუ ნორმალურიდან-ნორმალურამდე ინტერვალი ესაა სინუსის კვანძიდან გამოსული QRS კომპლექსებს შორის ყველა ინტერვალი [56].) ავტორებს ღამის პერიოდში ამ მაჩვენებლის შემცირება რისკის დამოუკიდებელ მარკერად მიაჩნიათ. ღამის საათებში გულის ცემის სიხშირის ცვლილების დაბალ ხარისხს ბრუგადას სინდრომის დროს პარკუჭოვანი ფიბრილაციისაკენ მიდრეკილების საფუძვლად მიიჩნევენ [57]. ბრუგადას სინდრომის კლინიკა და დიაგნოსტიკა: ანამნეზი: ავადმყოფს შეიძლება ჰქონდეს დაუდგენელი მიზეზის სინკოპეს ეპიზოდები, უეცარი სიკვდილის მორეციდივე შემთხვევები. ზოგი ავადმყოფი წარმატებითაა რეანიმირებული. შეტევა უხშირესად ღამის საათებში ან მოსვენების დროს ვითარდება. მამაკაცებში რვაჯერ უფრო ხშირია. უფრო მეტად 35-40 წლის ასაკში ვითარდება, თუმცა აღწერილია დიდი გადახრებიც ამ ფარგლებიდან. ანამნეზით უნდა დადგინდეს მემკვიდრეობაში გულისმიერი უეცარი სიკვდილის შემთხვევები მშობლებში ან და-ძმაში ახალგაზრდა ასაკში. გულის მხრივ სხვა ჩივილები არ აღინიშნება. ელექტროკარდიოგრაფიული გამოკვლევა: ამჟამად რეკომენდირებულია განიხილებოდეს სამი ტიპის ეკგ [9] იხ. სურათი #3. სურ. #3 ბრუგადას სამი ტიპის ეკგ.
I ტიპი- აღწერილია ბრუგადების მიერ 1992 წ [1]. აღინიშნება V1V2V3 განხრებში ST სეგმენტის ამოზნექილი, თაღის მაგვარი ელევაცია; J კბილის ამპლიტუდის ან ST სეგმენტის აწევა 2 მმ ან მეტად, მოჰყვება უარყოფითი T კბილი. II ტიპი- იმავე განხრებში ადგილი აქვს უნაგირის ფორმის ST სეგმენტის ელევაციას, J კბილის ამპლიტუდა 2 მმ ან მეტია, საწყისს აძლევს ST–ს დაღმავალ ელევაციას, რომელიც იზოხაზიდან ერთი მმ ან მეტია, მოყვება დადებითი ან ორფაზიანი T კბილი. III ტიპი- იგივე განხრებში შთ ელევაციას აქვს უნაგირის ან თაღის ფორმა, ან ორივე და ნაკლებია 1 მ/მ-ზე. სურათზე წარმოდგენილი ეკგ ეკუთვნის რეანიმირებულ ავადმყოფს ბრუგადას სინდრომით. ავტორები მიუთითებენ, რომ რეანიმაციის ჩატარებიდან პირველი საათების განმავლობაში ან უშუალოდ კარდიოვერტედეფიბრილატორის ჩართვის შემდეგ ჩაწერილი ეკგ არ შეიძლება გამოდგეს ბრუგადას სინდრომის სადიაგნოსტიკოდ. QT ინტერვალი უხშირესად ნორმის ფარგლებშია, თუმცა არის მონაცემები მისი გახანგრძლივების შესახებ პრეკორდიალურ განხრებში [58]. გამტარებლობის დარღვევის არასპეციფიურ ნიშნად მიიჩნევა განიერი S კბილები I, II, და III განხრებში, რაც ღერძის მარჯვნივ გადახრას იძლევა. ჰისის კონის მარჯვენა ან მარცხნივ გადახრასთან ერთად ან მის გარეშე. PR ინტერვალი ხშირად გაზრდილია და 200 მწმ უდრის ან აღემატება, და როგორც ჩანს HV გამტარებლობის შეფერხებას (55 მწმ) ასახავს. პედიატრიულ პრაქტიკაში დიაგნოსტიკას განსაკუთრებული როლი უნდა დაეთმოს გულმკერდის განსხვავებული აღნაგობის, მარჯვება პარკუჭის ძალების ასაკით განპირობებული უპირატესობის და საკონტროლო მონაცემების ნაკლებლობის გამო [9]. არსებობს მონაცემები [59], რომ ბრუგადას სინდრომის დროს ხშირია მოციმციმე არითმიის შემთხვევები (38%), აგრეთვე საკონტროლო ჯგუფთან შედარებით გახანგრძლივებულია წინაგულთაშორის გამტარებლობის დრო. წინაგულოვანი არითმიები Bordachar et.al მონაცემებით პაციენტთა 20%-ს აღმოაჩნდა [60]. მედიკამენტური დიაგნოსტიკა: ტარდება ეკგ-ზე ბრუგადას ტიპის ნიშნების გამოწვევის მიზნით, როდესაც ეკგ-ზე არაატიპიური ნიშნები და პაციენტს აქვს რომელიმე სიმპტომი: სინკოპე, რითმის პარკუჭოვანი დარღვევების ეპიზოდები, ოჯახური ანამნეზი, ცალკე ან ნებისმიერ კომბინაციაში. ინტრავენურად შეყვანილ პრეპარატებს შეუძლიათ გამოიწვიონ როგორც შთ სეგმენტის ელევაციის მომატება, ისე მისი გაჩენა. ტესტისთვის გამოიყენება ნატრიუმის არხის რომელიმე ბლოკატორი- აიმალინი (შეყავთ 1 მგ/კგ წინაზე 10 მგ/წთ სიჩქარით), ფლეკაინიდი (2 მგ/კგ წინაზე, მაქსიმალურად 150 მგ 10 წთ განმავლობაში) ან პროკაინამიდი (10მგ/კგ წინაზე 100მგ/წთ). ტესტის ჩატარების დროს აუცილებლია ეკგ 12 განხრის, სისხლის არტერიული წნევის მონიტორირება, რეანიმაციული ღონისძიებებისათვის მზადყოფნა. პრეპარატის შეყვანის შეწყვეტა ხდება დადებითი ტესტის შემთხვევაში ან პარკუჭოვანი ადრეული კომპლექსების ასევე პარკუჭოვანი ტაქიკარდიის გაჩენის ან Qღშ კომპლექსის 30%-ზე მეტად გაგანიერების დროს. დადებით ტესტად ითვლება: 1) J კბილის ამპლიტუდის მატება 2 მმ-ზე ზევით იზოხაზიდან V1 V2 V3 განხრებში, ან ერთ-ერთ მათგანში ჰისის კონის მარჯვენა ფეხის ბლოკადასთან ერთად ან მის გარეშე. 2) ბრუგადას II და III ტიპის ეკგ-ს გადასვლა I ტიპში. I ტიპის ეკგ-ს მქონე პაციენტების ტესტირებას დამატებით ღირებულებები არა აქვს. მხოლოდ J კბილის ამპლიტუდის გაზრდა 2 მმ-ზე მეტად I ტიპის კონფიგურაციაში გადასვლას გარეშე მნიშვნელოვნად უნდა განიხილებოდეს, თუმცა ეს ავტორთა გამოცდილებით იშვიათად ხდება. არადამაჯერებლად მიიჩნევა III ტიპის გადასვლა II ტიპში. ეკგ მონიტორირება რეკომენდებულია მის ნორმალიზებამდე. სერიოზული პარკუჭოვანი არითმიის დაწყებისთანავე პრეპარატის შეყვანა წყდება და იწყებენ ი/ვ იზოპროტერენოლის ინფუზიას (1-3 მიკროგრამი წუთში სიჩქარით) [9]. აიმალინის ტესტის ღირებულების დასადგენად ბრუგადას სინდრომს სადიაგნოსტიკოდ ჩატარდა მრავალცენტრიანი კვლევა [39]. გამოიკვლიეს 147 პაციენტი ოთხი დიდი ოჯახიდან, სადაც SCN5A გენის მუტაცია აღინიშნებოდა. აქედან 104 პაციენტი განისაზღვრა, როგორც ბრუგადას სინდრომის შესაძლო მქონე. 24 მათგანს უკვე საწყისი ეკგ-ზე ჰქონდათ ბრუგადას სინდრომის ნიშნები. აიმალინის ინტრავენურმა ინფუზიამ 35 გენის მატარებლიდან 28 შემთხვევაში დადებითი შედეგი გამოიღო, ხოლო უარყოფითი 7 შემთხვევაში. ტესტის მგრძნობელობა შეფასდა როგორც 80%, სპეციფიურობა 94,4%. ავტორთა აზრით SCN5A გენის სავარაუდოდ მაღალი მუტაციის რისკზე მიუთითებს I ხარისხის ატრიოვენტრიკულური ბლოკადა, როცა ბუნებრივია არ აღინიშნება შთ სეგმენტის ელევაცია. აიმალინის ტესტის ინფორმატიულობაზე და უსაფრთხოებაზე მიუთითებენ Rolf.et.al [61], რომელთაც გამოკვლეული 18 პაციენტიდან პარკუჭოვანი ტაქიკარდია მხოლოდ 1,3%-ში დააფიქსირეს. გარდა ზემოთ აღნიშნულისა პრეპარატებისა, სადიაგნოსტიკო ტესტად გამოყენებული იქნა კიდევ ერთი ნატრიუმის არხის ბლოკატორი-პილსიკაინიდ ქლორიდი, რომელმაც გამოიწვია არა მარტო ST სეგმენტის ელევაცია, არამედ პარკუჭოვანი ტაქიკარდია (უსიმპტომო პაციენტებში 7%, ხოლო სიმპტომიან პაციენტებში 60%-ში) და T კბილის ცვლილებები. [62]. არსებობს მონაცემები ციკლური ანტიდეპრესანტების ჭარბი მიღებით გამოწვეული ინტოქსიკაციის დროს ბრუგადას ტიპის ეკგ-ს განვითარებას შესახებ შემთხვევათა 15,3%-ში. სისხლში პრეპარატის კონცენტრაციის შემცირების კვალობაზე ეკგ საწყისს უბრუნდებოდა [63]. ელექტროფიზიოლოგიური გამოკვლევა. გვეხმარება რისკის ხარისხის დადგენაში, ზოგიერთ შემთხვევაში დიაგნოსტიკაში. რეკომენდირებულია ჩატარდეს გამოკვლევის პროტოკოლი სტიმულაციის ორი ადგილის გამოყენებით-მარჯვენა პარკუჭის მწვერვალი და მარჯვენა პარკუჭის გამოსასვლელი ტრაქტი, სულ მცირე სამი ხანგრძლივობის ციკლი (600, 430 და 330 მ.წმ) 1,2 და 3 ექსტრასტიმულით. გამოკვლევის ჩატარება სასურველია აგრეთვე იმ უსიმპტომო პაციენტებში, რომელთაც უეცარი გულისმიერი სიკვდილის ოჯახური ანამნეზი აქვთ [9]. 34 პაციენტზე ჩატარებული პროგრამირებული პარკუჭოვანი სტიმულაციის შედეგად 22 შემთხვევაში განვითარდა პარკუჭთა ფიბრილაცია და საჭირო გახდა პირდაპირი კარდიოვერსია, ხოლო დანარჩენ შემთხვევებში ფიბრილაციას ადგილი არ ჰქონდა. 38 თვის დაკვირვების შემდეგ ორივე ჯგუფში თანაბარი სიხშირით გამოვლინდა გულისმხრივი მოვლენები კარდიოვერტდეფიბრილატორით დაფიქსირებული პარკუჭთა ფიბრილაცია ან უეცარი გულისმიერი სიკვდილი [64]. P.Brugada at al [65]- თვლიან, რომ პარკუჭოვანი სტიმულაციის საჭიროება არის შემდეგი პირობების დროს: 1. უსიმპტომო ოჯახის წევრებში ნორმალური ან სპონტანური I ტიპის ეკგ დროს, როგორც უარყოფითი, ისე დადებითი ფარმაკოლოგიური ტესტის შემთხვევაში. 2. უსიმპტომო პირების სკრინინგის დროს, III, II ან I ტიპის სპონტანური ეკგ-ს შემთხვევაში როგორც დადებითი ისე უარყოფითი ფარმაკოლოგიური ტესტის დროს. პროგრამული პარკუჭოვან სტიმულაციას არ საჭიროებენ 1. სპონტანური პარკუჭოვანი ფიბრილაციის შემდეგ რეანიმირებულები ჯანმრთელი გულით, ნორმალური ეკგ-თი, როგორც დადებითი, ისე უარყოფითი ფარმაკოლოგიური ტესტით. 2. უცნობი მიზეზის სინოკოპეთი პაციენტები ჯანმრთელი გულით, სპონტანური I ტიპის ეკგ-თი ან ნორმალური ეკგ-თი, რომელთაც ფარმაკოლოგიური ტესტი დადებით ან უარყოფითი აქვთ. ბრუგადას სინდრომის დიაგნოზი. სერიოზულად უნდა განიხილებოდეს შემდეგ შემთხვევებში [9]: 1. თაღის ფორმის, I ტიპის ST სეგმენტის ელევაცია ერთ ან მეტ მარჯვენა პრეკორდიალურ – V1 V2 V3 განხრებში ნატრიუმის არხის, რომელიმე ბლოკატორის მოქმედების პირობებში ან მის გარეშე და ბრუგადას სინდრომის ერთი ქვემოთ ჩამოთვლილი მაჩვენებელი: - პარკუჭთა ფიბრილაციის დოკუმენტირებული შემთხვევა; - თავისით შეწყვეტილი პოლიმორფული პარკუჭოვანი ტაქიკარდია; - უეცარი გულისმიერი სიკვდილის ოჯახური შემთხვევა 46 წელზე ნაკლებ ასაკში; - ბრუგადას I ტიპის ეკგ ოჯახის წევრებში; - ელექტროფიზიოლოგიური ინდუცირება; - სინკოპე; - ღამის აგონიური სუნთქვა; ეკგ ნიშნების დადგენა კლინიკური სიმპტომების გარეშე ფასდება, როგორც ბრუგადას ტიპის ეკგ და არა როგორც ბრუგადას სინდრომი. 2. საწყის მდგომარეობაში უნაგირის ფორმის II ტიპის ეკგ ერთ ან მეტ პრეკორდიალურ განხრაში და მისი გადასვლა I ტიპში ნატრიუმის არხის ბლოკატორის მოქმედებით განიხილება, როგორც ზემოთ აღწერილი შემთხვევა. ბრუგადას სინდრომის სადიაგნოსტიკოდ საჭიროა ამას დაემატოს ზევით ჩამოთვლილი სიმპტომებიდან ერთი ან მეტი. 3. საწყის მდგომარეობაში III ტიპის ეკგ ერთ ან მეტ პრეკორდიალურ განხრაში და მისი გადასვლა I ტიპში ნატრიუმის არხის ბლოკატორის მოქმედებით ასევე განიხილება როგორც I შემთხვევა. აქაც სავალდებულოა ერთ-ერთ ზევით ჩამოთვლილი სიმპტომი, რათა ბრუგადას სინდრომის დიაგნოზი დადგინდეს. მედიკამენტით გამოწვეული III ტიპის გადასვლა II-ში, როგორც ზევით აღინიშნა, არადამაჯერებლად ითვლება. ის პაციენტები, რომლებიც მთლიანად არ აკმაყოფილებენ შემო-თავაზებულ ეკგ კრიტერიუმებს (მაგ. I ტიპის ეკგ J კბილის ამპლიტუდით 1 მმ), მაგრამ აქვთ ერთი ან მეტი კლინიკური სიმპტომი, სერიოზულად უნდა იქნენ შეფასებულები. ზევით ჩამოყალიბებული სადიაგნოსტიკო კრიტერიუმები არის ევროპის და ამერიკის კვლევით ცენტრების შეთანხმებული რეკომენდაცია ბრუგადას სინდრომის დიაგნოსტიკისათვის. გარდა ამისა არსებობს კვლევათა სხვა მონაცემებიც. ასე მაგალითად მიუთითებენ დამატებითი, ზედა ნეკნთაშუა განხრების (V1 V2 V3) - ინფორმატიულობაზე [66]. მონაცემები სამი მამაკაცის სპონტანური ან ინდუცირებული პარკუჭოვანი ფიბრილაციის შემთხვევის შესახებ, რომელთაც J კბილის და ST სეგმენტის ელევაცია გულმკერდის ქვედა განხრებში ჰქონდათ და გულის ორგანული დაზიანება არ აღენიშნებოდათ, წარმოადგინეს TagaKi et al [67] სამივე პაციენტს სინკოპე ღამის ან ადრე დილის საათებში უვითარდებოდათ. დიზოპირამიდის შეყვანა ST სეგმენტის ელევაციას ზრდიდა. ავტორები თვლიან, რომ აღწერილი შემთხვევა ძალზედ წააგავს ბრუგადას სინდრომს და შესაძლოა მის ვარიანტს წარმოადგენდეს. ანალოგიურ შემთხვევას აღწერენ პაციენტზე, რომელსაც პარკუჭთა ფიბრილაცია ინდუცირებული ჰქონდა ელექტროფიზიოლოგიური გამოკვლევით, ეკგ-ზე აღენიშნებოდა J კბილი და ST სეგმენტის ელევაცია ქვედა განხრებში, რომელიც იცვლებოდა დღეღამის განმავლობაში და მატულობდა ნატრიუმის არხის ბლოკატორის პილსიკაინიდის შეყვანის შემდეგ. პაციენტს არ ჰქონდა გულის სტრუქტურული დაზიანების ნიშნები. [68]. ასევე აღწერილია ვარიანტული ბრუგადას სინდრომი პაციენტზე, რომელსაც წარმატებული რეანიმაცია ჩაუტარდა პარკუჭოვანი ფიბრილაციის შემდეგ და ეკგ-ზე J კბილის და ST სეგმენტის აწევა აღენიშნა არა პრეკორდიალურ, არამედ გულმკერდის ქვედა განხრებში [69]. პილსიკპინიდის შეყვანამ გამოიწვია ST სეგმენტის აწევა თაღის ფორმით პრეკორდიალურ განხრებში. გამოყოფილია ე.წ. მაღალი რისკის ეკგ კრიტერიუმები[70] 1. S კბილი ტოლია ან მეტია 80 მწმ. V1 განხრაში. 2. ST სეგმენტის ელევაცია V2 განხრაში 80 მწმ-ზე მეტად J წერტილიდან- რომელთაც პარკუჭთა ფიბრილაციისთვის 100%-იანი მგრძნობელობა აქვთ. დიფერენციული დიაგნოზი: შთ სეგმენტის ელევაცია შეიძლება ნორმალური ეკგ-ს ვარიანტი იყოს. სურ. #4 მოცემულია შემთხვევები.
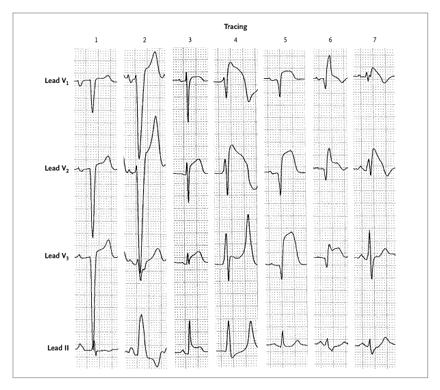
სურ.#4 ST სეგმენტის ელევაციას ნორმალური ვარიანტები [71] I სტრიქონზე ჩანს შთ სეგმენტის ელევაციის ნორმალური ვარიანტი. ახალგაზრდა ჯანმრთელ პირებს 90%-ში აღენიშნებათ შთ სეგმენტის აღმავალი ფორმით ელეცავია 1-3 მმ ფარგლებში. II სტრიქონზე ადრეული რეპოლარიზაციის ნიშნები. J წერტილის დაკბილვა, შთ სეგმენტის ელევაცია ჩაზნექილი ფორმით V4 განხრაში. თ კბილები შედარებით მაღალია. III სტრიქონზე ნორმალური ვარიანტი თ კბილის ინვერსიით, შთ ამოზნექილია, Qთ მცირდება. ამჟამად ფართოდაა ცნობილი ყველა ის პათოლოგიური მდგომარეობა, რომელიც შთ სეგმენტის ელევაციას იწვევს. მათ შედარება ბრუგადას ტიპის ეკგ-სთან მოცემულია სურ #5-ზე. სურ. #5 შთ სეგმენტის ელევაცია სხვადასხვა პათოლოგიის დროს [71]
ეკგ წარმოდგენილია V1V2V3 და III განხრებით. პირველი მწკრივი-მარცხენა პარკუჭის ჰიპერტროფია, მეორე ჰისის კონის მარცხენა ფეხის სრული ბლოკადა, მესამე-მწვავე პერიკარდიტი. შთ ელევაცია V2V3 და III განხრებში Pღ დეპრესია მეოთხე ჰიპერკალიემია-ფსევდოინფარქტული ცვლილებები. მაღალი წვეტიანი ვიწრო თ კბილი V3 განხრაში, მეხუთე გულის წინასეპტალური ინფარქტი. მეექვსე გულის წინასეპტალური ინფარქტი და ჰისის კონის მარჟვენა ფეხის სრული ბლოკადა ღ’ კბილი, შთ სეგმენტი ღ’–ის დაღმავალი ტოტიდან იწყება. და ბოლოს, მეშვიდე ბრუგადას სინდრომი რშღ’ თაღის ფორმის შთ ელევაცია V1V2 განხრებში. შთ სეგმენტი ღ წვეტიდან იწყება. ბრუგადას ტიპის ეკგ ცვლილებები შეიძლება გახდეს მიოკარდიუმის მწვავე ინფარქტის დიაგნოზის არასწორად დადგენის მიზეზი. ასეთი შემთხვევა მოყვანილია Aჰნ ეტ Hურსტ მიერ [72]. 55 წლის ტაილანდიელ მამაკაცს ეპიკარდიუმში მწვავედ განვითარებული დისკომფორტით და ბრუგადას მე-II ტიპის ეკგ-თი დაუდგინდა მიოკარდიუმის მწვავე ინფარქტის დიაგნოზი და დაეწყო თრომბოლიზური თერაპია. ეკგ-ზე ცვლილებები არ აღინიშნა, ამიტომ გადაყვანილი იქნა ქ. ატლანტის ემორის ჰოსპიტალში, სადაც ჩაუტარდა გულის კათეტერიზაცია. კორონარული არტერიოგრამა, და განდევნის ფრაქცია ნორმაში აღმოჩნდა, გულის ფერმენტები კვლავ ნორმაში რჩებოდა. პროკაინამიდის ინფუზიით გამოჩნდა გუმბათის ფორმის შთ სეგმენტის ელევაცია V2V3 განხრებში. საბოლოოდ პაციენტის ჩივილები შეფასდა, როგორც კუჭნაწლავის რეფლექსი. საჭიროდ არ ჩაითვალა მარჟვენა პარკუჭის ბიოფსიის და ელექტროფიზიოლოგიური გამოკვლევის ჩატარება. არც კარდიოვერტედეფიბრილატორის იმპლანტაცია და ანტიარიტმული პრეპარატების დანიშვნა. მნიშვნელოვანია გატარდეს დიფერეციული დიაგნოზი მარჟვენა პარკუჭის არითმოგენულ კარდიომიოპათიასა (მპაკ) და ბრუგადას სინდრომს შორის. [9] მპაკ უფრო ხშირად 25-35 წლის ასაკში გვხვდება. მამაკაცებში 3 ჟერ უფრო ხშირია. გავრცელებულია ყველგან უფრო ხშირად კი ჩრდილოეთ იტალიაში. ბრუგადას სინდრომი აღინიშნება 34-40 წლის ასაკში, მამაკაცებში 8 ჟერ უფრო ხშირია, ყველგან გვხვდება, უფრო ხშირად სამხრეთ აღმოსავლეთ აზიაში. მპაკ არის, როგორც აუტოსომურ დომინანტური, ისე აუტოსომურრეცისიული პათოლოგია, პროცესი მიმდინარეობს 1,2,3,10,13 ქრომოსამაში, ზიანდება HღYღ2 გენი, ბრუგადას სინდრომის გადაცემა ხდება აუტოსომურ-დომინანტურად, ზიანდება მე-3 ქრომოსომაში შჩN5A გენი. მპაკ შემთხვევაში ავადმყოფს აქვს გულისფრიალი, სინკოპე, გულის გაჩერება, ვითარდება დაძაბვის დროს, აღინიშნება მარჟვენა პარკუჭის (და მარცხენა პარკუჭის) მორფოფუნქციური დარღვევები. პათანატომიურად ფიბროზულ-ცხიმოვანი პათოლოგია. ეკგ-ზე ინვერტული თ კბილი პრეკორდიალურ განხრებში, ეფსილონ კბილი, მოგვიანებით წინაგულოვანი არითმიები. ბრუგადას სინდრომის დროს ავადმყოფს აქვს სინკოპე, გულის გაჩერება, ვითარდება მოსვენების დროს, გულის ფუნქციურ და მორფოლოგიურ დარღვევები არ აღინიშნება, ეკგ-ზე შთ ელევაცია V1V2V3 განხრებში, მარჟვენა ფეხის ბლოკადა, ღერძის მარცხნივ გადახრა Pღ/HV გახანგრძლივება 50%-ში, ადრეულ ეტაპზე წინაგულოვანი არიტმიები 10-25%-ში. მპაკ დროს ადგილი აქვს მონომორფულ პარკუჭოვან ტაქიკარდიას, ფიბრილაციას, მიმდინარეობს გულის უკმარისობით, უეცარი სიკვდილით, ბრუგადას სინდრომის დროს აღინიშნება პოლიმორფული პარკუჭოვანი ტაქიკარდია, ფიბრილაცია და უეცარი სიკვდილი. აღწერილია ბრუგადას სინდრომის დროს პარკუჭთა ფიბრილაციის დროული და წარმატებული მკურნალობის შემთხვევა [73]. პოლიციელმა თავისი მანქანის წინ მოძრავი მძღოლი, რომელიც ბარიერს შეეჟახა და გაჩერდა, ნახა კლინიკური სიკვდილის მდგომარეობაში. მან ადგილზე დაიწყო რეანიმაციული ღონისძიებები, ხოლო ადგილზე მისულმა პარამედიკოსებმა პაციენტს ჩაუტარდეს წარმატებული დეფიბრილაცია და გადაიყვანეს კლინიკაში. ბრუგადას სინდრომით დაავადებული პაციენტის ქირურგიული ოპერაციის შემთხვევაში საერთო ნარკოზის დროს სასურველია ჩატარდეს მონიტორირება, როგორც ოპერაციის, ისე მის შემდგომ პერიოდში, რათა არ გამოიპაროს პარკუჭოვანი არითმიის შემთხვევა [74]. მკურნალობა: იმპლანტირებული კარდიოვერტედეფიბრილატორი მიჩნეულია ბრუგადას სინდრომის ძირითად სამკურნალო საშუალებად [75]. ამავე მეთოდის გამოყენებაზე მიუთითებენ არა მარტო ბრუგადას სინდრომის, არამედ ნორმალური მექანიკური ფუნქციის პირობებში გულის ისეთ ელექტროფიზიოლოგიურ დარღვევების დროს როგორიცაა ჭPჭ სინდრომი, გახანგრძლივებული Qთ [76]. თუმცა ეს მეთოდი ვერ იქნება ადექვატური საშუალება პატარა ბავშვების, აგრეთვე მოზრდილების სამკურნალოდ იმ რეგიონებში, სადაც იმპლანტირებული კარდიოვერტედეფიბრილატორის გამოყენება ეკონომიურ პრობლემებთანაა დაკავშირებული. ბრუგადას სინდრომის პათოფიზიოლოგიიდან გამომდინარე ფარმაკოლოგიურ ზემოქმედება უნდა მიმართული იყოს მარჟვენა პარკუჭის ეპიკარდიუმში მოქმედების პოტენციალის ადრეული ფაზის აქტივობის ბალანსირებისაკენ. ამ თვალსაზრისით მიღებულია ქინიდინის და იზოპროტერენოლის გამოყენება [22,40,77,78]. ჩატარებულია ჰიდროქიდინით მკურნალობა 35 პაციენტზე, რომელთაც ბრუგადას სინდრომი აღენიშნებოდათ [79]. მათგან ოთხს ჩადგმული ჰქონდა კარდიოვერტედეფიბრილატორი, რომლის გამოყენება მრავალჟერ უხდებოდათ, დანარჩენები იყო უსიმპტომო პაციენტები, რომელთაც ელექტროფიზიოლოგიური გამოკვლევით ინდუცირებული ჰქონდათ პარკუჭოვანი არითმიები. ჰიდროქინიდით 17±13 თვის განმავლობაში მკურნალობის შედეგად პირევლი ჟგუფის ავადმყოფებს კარდიოვერტედეფიბრილატორის გამოყენება არ დასჭირვებიათ, ხოლო დანარჩენ შემთხვევებში 76%-ში თავიდან იქნა აცილებული პარკუჭოვანი ტაქიკარდიის და ფიბრილაციის ინდუცირება. ავტორები მიიჩნევენ, რომ ჰიდროქინიდინით პრევეციული მკურნალობა შეიძლება გახდეს იმპლანტირებულ კარდიოვერტედეფიბრილატორის ალტერნატივა იმ უსიმპტომო პაციენტებში, რომელთაც ინდუცირებული არითმია აქვთ. ქინიდინით მკურნალობის ეფექტურობაზე აგრეთვე მიუთითებენ Bელჰასსენ ეტ ელ [80], რომელთაც შეისწავლეს 25 პაციენტი ბრუგადას სინდრომით. ქინიდინის ბისულფატი 1483±240 მგ. დოზით ეძლეოდათ სპონტანური ან ინდუცირებული პარკუჭოვანი ფიბრილაციის პროფილაქტიკისათვის. ყველა ავადმყოფს ჩაუტარდა ელექტროფიზიოლოგიური კვლევა. ქინიდინმა პარკუჭოვანი ფიბრილაციის პრევენცია მოახდინა 88%-ში. ავტორები თვლიან, რომ საჭიროაა ღრმად იქნას შესწავლილი კარდიოვერტედეფიბრილატორით და ქინიდინით მკურნალობის შედარება. აღწერილია 67 წლის მამაკაცი ბრუგადას სინდრომით, რომელსაც პარკუჭოვანი ფიბრილაციის სრული პრევენცია ჩაუტარდა ფოსფოდიესთერაზის ინჰიბიტორის ცილოსტაზოლის პერორალურ დანიშვნის შემდეგ [81]. პაციენტს პარკუჭოვანი ფიბრილაციის ეპიზოდები მანამდე ზედიზედ ოთხი დღის განმავლობაში ადრე დილის საათებში ჰქონდა. იზოპროტერენოლის დაბალი დოზის შეყვანა ბრუგადას სინდრომით დაავადებულ პაციენტებში სწრაფად აცილებდა პარკუჭთა ფიბრილაციის შეტევებს, ხსნიდა ადრეულ პარკუჭოვან შეკუმშვებს და ეკგ-ს ნორმალიზებასაც იწვევდა [82]. პროგნოზი: პროგნოზის დადგენაში ითვალისწინებენ მრავალ ფაქტორს- არის თუ არა მხოლოდ ბრუგადას ტიპის ეკგ, არის სინკოპეს ეპიზოდები, ოჟახური შემთხვევები და ა.შ. 212 პაციენტი, რომლებსაც არენიშნებოდათ ბრუგადას I ტიპის ეკგ დაყვეს სამ ჟგუფად: I-უსიმპტომო პაციენტები (123 ავადმყოფი) II-ერთი ან მეტი დაუდგენელი მიზეზის სინკოპეთი ანამნეზებში (65 პაციენტი) და III-24 ავადმყოფი რეანიმირებული პარკუჭთა ფიბრილაციის გამო [83], ბრუგადას I ტიპის ეკგ სპონტანურ იყო 125 შემთხვევაში. დანარჩენებში კი ფარმაკოლოგიური ტესტით გამოწვეული. 40-50 თვის დაკვირვების შემდეგ პირველი არიტმიის შემთხვევა I ჟგუფში 0,8%-ში აღინიშნა, ხოლო II და III ჟგუფებში კი მორეციდივე არითმია-შესაბამისად 6 და 17%-ში. ათწლიანი დაკვირვება ჩატარდა 69 უსიმპტომო პაციენტზე, რომელთაც პირველადად აღენიშნებოდათ ბრუგადას I და II ტიპის ეკგ, და ოჟახური ანამნეზით არ ჰქონდათ უეცარი გულისმიერი სიკვდილის შემთხვევები [84], პარკუჭოვანი ფიბრილაციის ეპიზოდები, მხოლოდ ერთ შემთხვევაში განვითარდა. ამრიგად, ეს ავტორები უსიმპტომო პაციენტებს ოჟახური ანამნეზის გარეშე დაბალი რისკის ჟგუფად მიიჩნევენ. ხანგრძლივი დაკვირვება ჩატარდა პაციენტთა სამ ჟგუფზე, რომელთაც V1V2V3 განხრებში შთ სეგმენტის ელევაცია და ჰისის კონის მარჟვენა ფეხის ბლოკადა აღენიშნებოდათ [85]. I ჟგუფში შედიოდა 71 რეანიმირებული, II ჟგუფში- ანამნეზში სინკოპეს მქონე 73 პაციენტი და III ჟგუფში 190 უსიმპტომო პაციენტი. ახალი არითმიის ეპიზოდები ჟგუფების შესაბამისად 62,19 და 8%-ში განვითარდა. 30 უსიმპტომო პაციენტზე ხანგრძლივი დაკვირვების შემდეგ დადგინდა [86], რომ აქ პარკუჭოვანი ფიბრილაცია არ განვითარებულა, ხოლო იგივე რაოდენობის (30 პაციენტი) სიმპტომებიან პაციენტებში დაკვირვების იგივე პერიოდში პარკუჭოვანი ფიბრილაცია 5 შემთხვევაში დაფიქსირდა. ზოგიერთი ავტორი, უსიმპტომო პაციენტებს ოჟახური ანამნეზის გარეშე, რომელთაც მე-2 ან მე-3 ტიპის ეკგ აქვთ ნორმალურ ვარიანტად მიიჩნევენ [16,87]. P. Bრუგადა-ს [88] მიხედვით რისკის ჟგუფები შემდეგნაირად უნდა განისაზღვროს-დაბალი რისკის ჟგუფი უსიმპტომო პაციენტები, რომელთაც მედიკამენტური ტესტით პათოლოგიური ეკგ გამოეწვევა. საშუალო რისკის ჟგუფი უსიმპტომო პაციენტები სპონტანური პათოლოგიური ეკგ-თი. მაღალი რისკის ჟგუფი-სინკოპეს ეპიზოდები, სპონტანური ან მედიკამენტური ტესტით გამოწვეული პათოლოგიური ეკგ-თი. დახმარების გარეშე უეჭველი სიკვდილის რისკის ჟგუფი-სპონტანური პათოლოგიური ეკგ და სპონტანური პარკუჭოვანი ფიბრილაცია. ლიტერატურა: 1. Brugada P. Brugada J. Right bundle branch block, persistent ST segment elevation and sudden cardiac death: a distinct clinical and electrocardiographic syndrome: a multicenter report. J.Am.Coll Cardiol. 1992,20:1391-1396. 2. Yan G.X., Autzelevitch C. Cellular basis for the electrocardiographic J wave. Circulation 1996; 93: 372-379. 3. Miyazaki T. Mitamura H, Miyoshi S. et al. Autonomic and autiarrhythmic drug modulation of ST segment elevaition in patient with Brugadas syndrome J Am. Coll.Cardiol. 1996; 27: 1061-1070 4. Martini B. Nava A. Thiene et. al. Ventricular fibrillation without apparent heart disease: discription ot six cases. Am. Heart J.1989; 118: 1203-1209 5. Autzelevitch C. Brugada P. Borggrefe M. Brugada syndrome: report of the second cousensus conference-Circulation 2005; 111: 659-670. 6. Farre. H - Presentation of secondary prevention of sudden death at 2002. Madrid arrhythmia meeting. 7. Huikuri H, Castellanoe A. Myerburg RJ.- Sudden death du to cardiac arrhythmias. N.Engl.J.Med. 2001, V345 (20):1473. 8. Antzelevitch C. Brugada P. Brugada J. et al Brugada syndrome. A decade of progress. Circ. Res. 2002; 91: 1114-1118. 9. Walde A. Antzelevitch C. Brugada M.at al. Proposed diagnostic criteria for the Brugada syndrome. Consensus report. Circulation. 2002,106:2514-2519. 10. Nimmanit S. Malasit P. Chaovakul V. at al. Pathogenesis of sudden unexplained nocturnal death (Lai tai) and endemic distal renal tububar acidosis. Laucet 1991 oct. 12, 338 (8772):930-932. 11. Gotoh K.A histopathological study on the conduction systen of the so-called “Pokkuri disease” (Sudden unexpected cardiac death of unknown origin in Japan) Jpn Circ J. 1976. Jul,40(7):753-768 12. Nademane K. VeeraKul G. NimmannititS etal. Arrhythmogenic marker for the Sudden unexplained death syndrome in Trai men. Circulaition. 1997. 96, 2595-2600. 13. Miyassaka Y. TsujiH, Yamada K.-Prevalence and mortality of the Brugada-type electrocardiogram in one city in Japan. J.Am.Coll. Cardiol. 2001,38,771-774. 14. AtarashiH, OgawaS. HarumiK. etal.- Three-year follow-up of patients with right bundle branch block and ST segment elevaition in the right precordial leads. Japanese registry of Brugada syndrome. J.Am.Coll. Cardiol.2001, 37:1916-1920. 15. Matsuo K. Akahoshi M. Nakashima T. et.al. The prevalence, incidence and prognostic value of the Bruguda-type electrocardiogram. A populaition-based study of four decades. J.Am. Coll. Cardiol. 2001; 38:765-770 16. Junttila M.J. Reatikainen MJP. Karjalainen J. Prevalence and prognosis of subjects with Brugada-type ECG pattern in a young and middle-age Finnish population-Eur. Heart J. 2004 V.25.n10.874-878 17. Дупляков Д.В. Блокада правой ножки пучка Гиса, подъем сегмента ST в отведениях V1 V2 (V3) и опасные для жизни нарушения сердечного ритма. Кардиология 2001, 8 93-96. 18. Макарова Л.М. Бругада П. Чупрова СН. и др. Клинико-электрокардиографические оссобенности синдроме Бругада (Клиничесое наблюдение семейнного случая и обзор литературы). Кардиология 2002, 94-100 19. Ватутин Н.Т. Склянная Е.В. – Синдром Бругада. Кардиология 2003 11. 80-85. 20. Chen Q. Kirsch G.E. Zhang D. et al- Genetic Basis and molecular mechanism for idiopathic ventricular fibrillation. Nature. 1998 Mar.19, 392 (6673) 293-296. 21. Brugada J.Brugada R. Brugada P.-Brugada syndrome Arch. Mal. Coeur. Vaiss 1999, 92 (7); 847-850 22. Antzelev-itch C. The Brugada syndrome: iconic basis and arrhythmia mechanisms. J.cardiovas. Electrphysiol 2001,12,268-272 23. Priori S. Napolitano C. Gasparini M. et al-Natural history of Brugada syndrome: Insights for risk stratification and menagment Cirgulation 2002, 105, 1342-1347 24. Dumaine J. Towbin A. Brugada P et al- Jonic Mechanisms responsible for the electrocardiographic phenotype of the Brugada syndrome are temperature dependent-Cir. Res. 1999, 85, 803-809 25. Kass R.- The channelopathies: novel unsights into molecular and genetic mechanisms of human disease. J. Clin. Juvest 2005, 115; 1986-1989 26. Royer A. Van Veen T. LeBouter S. et al- Mouse model of SCN5A linked hereditary Lenegre’s disease. Age-related conduction Slowing and myocardial fibrosis. Circulaition 2005 111.1738-1746. 27. Kyndt F. Probst V. Potet F. et al-Novel SCH5A mutation leading either to isolated Cardiac condition defect or Brugada syndrome in a large french family. Circulaition 2001, 104; 3081-3086. 28. Fish JM. Antzelevitch C.-Cellular and ionic basis for sex-related difference in the manifestation of the Brugada syndrome and progressive coudiction desease phenotypes-J.Elctrocardiol 2003,96 suppl. 173-179. 29. Roberts R. Brugada R-Genetics and arrhythmias- Annu. Rev. Med. 2003, 54. 257-267 30. Delisle B.Anson B. Bajamani S. et al- Biology of cardiac arrhythmias. Circulaition 2004. 94, 1418-1428. 31. Wellens H. Gorgels A.- The electrocardiogram 162 yaers after Einthoven. Circulaition 2004, 109, 562-564. 32. Brugada R. Genetic bases of arrhythmias- Rev. Esp. Cardiol. 1998 51 (4) 274-285. 33. Wang Q. Shen J. Splawski J et al SCN5A mutations associated an inherited cardiac arrhythmis, long QT syndrome. Cell. 1995-10, 80(5).805-811 34. Bezzina C. Veldcamp M. vanden Berg M et al-A single Na+ channel mutation causing both long –QT and Brugada syndromes. Circ. Res. 1999. 85, 1206-1213 35. Veldkamp M. Viswanathas P. Bezzina C et al- Two distinct congenital Arrhythmias Evoked by a multidysfunctional Na+ Channel-Circ. Res. 2002,86;1008. 36. Beaufort-Krol G. van den Berg M. Wilde A et al- Developmental aspects of long QT type 3 and Brugada syndrome on the basis of single SCN5A mutaition in childhood J.Am.Coll.Cardiol 2005,46,331-337. 37. Weiss R. Brugada M. Nguyen T. et al-Clinical and molecular heterogeneity in the Brugada syndrome. A novel Gene locus on chromosome 3 Circulation 2002, 105, 707-713 38. Akai J. Makita N. Saknrada H. et al.- A novel SCN5A mutation associated with idiopathic ventricular fibrillation without typical ECG finding of Brugada syndrome. FEBS. lett. 2000, 11,479(1-2); 29-34 39. Hong K. Berruezo-Sanchez A. Poungvarin N et al.-Phenotypic characterization of large European family with Brugada syndrome displaing a sudden unexpected death syndrome mutation in SCN5A J. Cardio vasc Electrophysiol. 2004, 15(1)70-71 40. Yan G.X. Antzelevitch C. Cellura basis for the Brugada syndrome and other mechanisms of arrhythmogenesis associated with ST segment elevation-Circuletion 1999, 100,1660-1666. 41. Hlaing T. Di Mino T. Kowey PR et al- ECG repolarization waves: This genesis and clinical implicaition Ann Noninvasive Electrocardiol 2005,10 211-223. 42. Hurst J.W. Naming of the waves in the ECG with a brief Account of their genesis Circulaition 1998,98,1937-1942 43. Погвизд С.- Анализ ЭКГ ст 183. В « Кардиогия в таблицах и схемах» . Москва 1996 44. Alings M. Wilde A.- Brugada syndrome. Clinical data and Suggested pathophysuological mechanism Circulaition 1999. 99,666-673 45. Litovsky SH. Antzelevitch C.-Rate dependence of action potential duraition and refractoriness in canine ventricular endocardium differs from that of epicardium: role of the transient outward current. J. Am.Coll Cardiol 1989 14(4) 1053-1066 46. Kurita T. Shimizi W. Jnagaki M. et al- The electrophisiologic mechanism of ST segment elevation in Brugada syndrome. J.Am.Col Cardiol. 2002,40,330-334. 47. Ramon Brugada Foudation- Brugada syndrome-Relation with “Early Repolarisaition”-site supported by Mapfre Foundation. 48. Kakishita M. Kurita T. Matsuo K.-Mode of onset of ventricular fibrillation in patients with Brugada syndrome detected by implantable cardioverter defibrillator therapy- J.Am.Coll.Cardiol. 2000, 36, 1646-1653. 49. Tukkie R. Sogaard P. Vleugels J. et.al- Delay in right ventricular activaition cintributes to Brugada syndrome- Circulaition 2004;109;1272-1277. 50. KasannKi H. Ohnishi S. OhtuKa M. et al- Idiopathic ventricular fibrilaition induced with vagal activity in patients without obvious heart desease.- Circulaition 1997, 9; 2277-2285. 51. Wichter T. Matheja P. Eckardt l et al- Cardiac autonomic dysfunction in Brugada syndrome-Circulaition 2002,105 702-706 52. Shimizu W. KamaKura S.-Catecholamines in children with congenital long QT syndrome and Brugada syndrome J. Electrocardiol. 2001.34,(suppe) 173-175. 53. Wicter T. Shafers M. Rhodes C. et al- Abnormalitis of cardiac sympatheitic innervation in arrhythmogenic right ventricular cardiomyopathy. Circulaition 2000, 101, 1552-1558 54. Noda T. Shimizi W. Taguchi A et al – ST segment elevaition and ventricular fibrilaition without coronary spasm by intracoronary injection of acetylcholine and /or ergonovine maleate in patients with Brugada syndrome J. Am.Coll. Cardiol. 2002,40: 1841-1847 55. Hermida J.S. Leenhardt A. Cauchemez B-Decreased nocturnal standard deviation of averaged N.N. intervales Eur. heart. J 2003,v34.n22.2061.2069. 56. TasK Force of European Society of cardiology the North American Society of pacing Electrophysiology- Heart rate Variability Circulaition 1996,93, 1043-1065. 57. Krittayaphong R. VeeraKul G. Nademane K et al- Heart rate variability in patients with Brugada syndrome in Thailand Eur. Heart. J. 2003 v.24.n19,1771-1778 58. Pitzalis M. Anaclerio M. Jacoviello M. –QT interval prolongation in right precordial leads. J.Am. Coll. Cardiol. 2003,42,1632-1637 59. Morita H. Kusano-FuKushima K. Nagase S. et al- Atrial fibrillaition and atrial vulnerability in patients with Brugada syndrome. J.Am. Coll. cardiol. 2002 40;1437-1444. 60. Bordachar P. Reuter S. Garrigue S et al- Insidence, clinical implicaition and prognosis of atrial arrhythmias in Brugada syndrome, Eur.Heart J.2004; 25; 879-884 61. Relf S. Bruns H.J. Wichter T. et al- The ajmaline challenge in Brugada syndrome: diagnostic impact, safety and recommended protocol. Eur. Heart J.2003, v.24,N12.1104-1112 62. Morita H. Morita S.T. Nagase S et al- Ventricular arrhythmia induced by sodium channel blocer in patients with Brugada syndrome. J.Am. Coll. cardiol. 2003. 42,1624-1631. 63. Goldgran-Toledano D. Sideris G. KevorKian J.- Overdose of cyclic antidepressants and Brugada syndrome N.Engl.J. Med.2002,346,1591-1592 64. Kanda M. Shimizn W. Matsuo K. et al- Electrophisiologic characteristics and implicaitions of induced ventricular fibrilation in symptomatic patients with Brugada syndrome J.Am. Coll.Cardiol. 2002.39, 1799-1805 65. Brugada P. Brugada R. Brugada J. Should patients with an asymptomatic Brugada electrocardiogram undergo pharmacological and electrophisiological testing? Circulaition 2005,112, 279-292 66. Sangwatanaroj S. Preshawat S. Sunsaneewi, tayakul B. et al- New electrocardiographic leads and the procainamide test for the detection of the Brugada sigh in sudden unexplained death syndrome survivors and their relatives. Eur. Heart J. 2001, v.22.n.24.2290-2296. 67. Takagi M.Aihara N. Takaki et al- Clinical characteristics of patients with spontaneous or inducible ventricular fibrillaition without apparent heart diseases presenting with J wave and ST segment elevaition in inferior leads. J. Cardiovasc.Electrophysiol.2000.11,844-848 68. Sahara M. Sagara K. Yamashita T et al- J wave and ST segment elevaition in the inferior leads: a latent type of variant Brugada syndrome? Jpn Heart J 2002 43,55- 60. 69. Ogawa M. Kumagai K. Yamanouchi Y. et al- Spoteneous onset of ventricular fibrillaition in Brugada syndrome with J wave ans ST segment elevaition in the inferior leads. Heart Rhythm 2005,2,97-99. 70. Atarashi H. Ogawa S.-New ECG criteria for high risk for the idiopathic ventricular fibrillaition- Br.S.Circ.J.2003,67,8-10. 71. Wang K. Asinger R, Marriott H,- ST segment Elevaition in conditions other than acute myocardial infarction. N.Engl.J.Med. 2003,v.349,2128-2135 72. Ahn J, Hurst J.W. – Worrisome thought about the diagnosis and treatment of the patients with Brugada waves and the Brugada syndrome. Circulation 2004,109,1463-1467. 73. Butler J. Brugada syndrome- the missed epidemic. J Accid Emerg Med. 2000, 17, 426-428 74. Santamborogio L. Mencherini S. Fuardo M. et al- The surgical patient with Brugada syndrome four-case clinical Experience-Anesth.Amalg. 2005,100;1263-1266 75. Brugada P.BrugadaR. BrugadaJ et al- Use of the prophylactic implantable cardioverter defibrillator for patients with nornal heart- Am. J. Cardiol 1999,83;98-100. 76. Wever E. Robles de Medina E-Sudden death in patients without structural heart disease. J.Am. Coll. cardiol. 2004,43,1137-1144. 77. Alings M. Dekkert L. Sadee A et al- Quinidine induced electrocardiographic normalizaition in two patients with Brugada syndrome-Pacing Clin Electrophisiol 2001.sep.24.1420-1422 78. Tanaka H.Kinoshita O. VchikawaS-Successful prevention of recurent ventricular fibrillation by intravenous isoprotenol in a patient with Brugada syndrom. Pacing Clin. Electrophisiol.2001.24;1293-1294. 79. Hermida J.S.Denjoy J. Clerc J.et al- Hydroquinidine theraphy in Brugada syndrome-J.Am.Coll. cardiol 2004.43.1853-1860 80. Belhassen B Glick A.ViskinS. Efficay a quinidine in high-risk patients with Brugada syndrome - Circulaition 2004,110. 1731-1737 81. Tsuchiya T.Ashikaga K. Honda T. et al- Prevention of ventricular fibrillaition by cilostazil, anoral phosphodies-terase inhibitor, in patient with Brugada syndrom J.Cardiovasc Electrophisiol. 2002 13(7) 698-701 82. Maury P. Coudere P. Deby et al- Electrical storm in Brugada syndrom successfully an oral treated using isoprenalineEuropace 2004,mar 6(2)130-133. 83. Ekardt L. Probst V.Smits J. Lomg-term Prognosis of individual with right precordial ST segment Elevaition Brugada syndrome-Circulaition 2005 111,257-263 84. Sakabe M. Fujiki A. Tani M.- Proportion and prognosis of healthy people with coved or saddle-back type ST segment elevation in right precordial leads during 10 years follow up. Eur.Heart J 2003,vol.24.n.16.1488-1493 85. Brugada J. Brugada R. Antzelevitch C.-Long-term follow up of individual with the electrocardiographic pattern of righ bundel-branch block and ST segment elevaition in precordial leads V1 to V3-Circulaition 2002, 105,73-78 86. Priori S. Napolitano C. Gasparini M.-Clinical and genetic heterogenity of right bundele branch block and ST segments elevaition syndrome. Circulaition 2000, 102,2509-2515; 87. Littman L. Monroe M. Kerns W- Brugada syndrome and “Brugada sign” Clinical spectrum with a guide for the clinician-Amer. Heart J.2003, v.145n.5: 768-778. 88. Brugada P.-Spectrum of clinical presentaition and prognosis in Brugada syndrome. Aalst. Belgium.Sept 2000. |