|
პერიფერიულ სისხლში ჩD34, ჩD133+,
ჩD34- და მ.როგავა ზ.ღურწკაია - თერაპიის ეროვნული ცენტრი |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
ექსპერტების შეფასებებზე დაყრდნობით, სიმპტომატური გულის უკმარისობა ევროპის პოპულაციაში 0.4 დან 2%-მდე მერყეობს [1]. გულის უკმარისობის შემთხვევები სწრაფად იზრდება ასაკთან ერთად [2]. პაციენტების საშუალო ასაკი 74 წელს აღწევს [3,4,5]. აღინიშნება გულის უკმარისობით სიკვდილობის განუხრელი ზრდა ყველა ასაკოვან კატეგორიაში. ევროკავშირში შემავალ ქვეყნებში სულ 900 მილიონი ადამიანი ცხოვრობს, მათგან დაახლოებით 10 მილიონი გულის უკმარისობით არის შეპყრობილი, დაახლოებით ამდენივეს აღენიშნება მიოკარდიუმის დისფუნქცია უკმარისობის კლინიკური ნიშნების გარეშე [6,7]. დაავადების ადექვატური კორექციის შეუძლებლობის შემთხვევაში, რაც საფუძვლად უდევს გულის უკმარისობის ჩამოყალიბებას, სტადიის მიუხედავად ხასიათდება არაკეთილსაიმედო პროგნოზით. პაციენტების ნახევარი კვდება დიაგნოზის დასმიდან პირველი 4 წლის განმავლობაში. მძიმე გულის უკმარისობისას პაციენტების ასეთივე რაოდენობა კვდება პირველი წლის განმავლობაში. ბოლო წლების კვლევებმა აჩვენა, რომ პაციენტები მიოკარდიუმის ასიმპტომური დისფუნქციით ასევე ხასიათდებიან არაკეთილსაიმედო პროგნოზით. გულის ქრონიკული უკმარისობა ადრეულ სტადიაზე თითქმის ავადმყოფთა 40%-ში უსიმპტომოდ მიმდინარეობს. ამასთან ერთად პაციენტების ყოველწლიური სიკვდილობა გულის უკმარისობის I ფუნქციონალური კლასითაც (NYHA) კი 10-12%-ს შეადგენს. დღეისათვის გულის უკმარისობის სამკურნალოდ პრეპარატების ფართო სპექტრსა და არამედიკამენტოზური მკურნალობის სხვადასხვა მეთოდებს იყენებენ, ამასთან ერთად პოპულაციაში მისი განვითარების სიხშირე და გავრცელება კვლავ იზრდება. ყოველივე ზემოთქმულიდან გამომდინარე დღის წესრიგში დადგა გულის უკმარისობის სამკურნალოდ პრინციპულად ახალი მიდგომების ძიების პრობლემა. აქტუალური გახდა რეგენერაციული მედიცინის განვითარების საკითხი, რომლის პირველმა გარკვეულმა მიღწევებმა ასახვა ჰპოვა 60-იანი წლების მეცნიერთა შრომებში. პოლეჟაევი თავისი მონოგრაფიის “Регенерация сердечной мышцы” შესავალ ნაწილში წერდა: “ორგანიზმისათვის სულ ერთი არ არის, დაზიანებულ მიოკარდიუმს შემაერთებელი ქსოვილი ჩაენაცვლება თუ მოხდება მისი რეპარაციული რეგენერაცია (დეფექტის უბნის ახალი კარდიომიოციტებით ჩანაცვლება), ფუნქციის სრული აღდგენით” [8]. კარდიომიოციტების რეპროდუქციული უნარის არარსებობა დიდი ხანია ცნობილი ფაქტია. გულის კუნთის დეფექტის ჩანაცვლება ხდება ძირითადად სტრომის უჯრედების (ფიბრობლასტების) პროლიფერაციის შედეგად [9]. ითვლება, რომ თუ განვითარდა მიოკარდიუმის ინფარქტი, ის შეუქცევადია და იწვევს გულის კუნთის რემოდელირებას, რაც ხშირად რამოდენიმე თვეში ან წელიწადში გულის უკმარისობის განვითარებით მთავრდება [10], რომლის ტერმინალურ სტადიაზე მკურნალობის ერთადერთ რადიკალურ მეთოდს გულის ტრანსპლანტაცია წარმოადგენს. ამასთან ერთად, უკანასკნელ წლებში გაჩნდა მონაცემები მიოკარდიუმის რეგენერაციული უნარის შესახებ. გულის კუნთის რეპროდუქციული უნარი გაანალიზეს Kajstura et al. (1998) [11] გულის ტრანსპლანტაციის გადატანილ და დილატაციური კარდიომიოპათიით დაავადებულ პაციენტებში, კარდიომიოციტების მიტოზური ინდექსის განსაზღვრის გზით. ამ ავტორების მიერ ჩატარებულმა გამოთვლებმა გვიჩვენა, რომ თუ 45 წლის ჯანმრთელი ადამიანის წინაგულში საშუალოდ 5.8X109 ბირთვია, ხოლო მიტოზური ინდექსი შეადგენს 14-ს 106-ზე, მაშინ 2X103 კარდიომიოციტის ბირთვი მიტოზის სტადიაში იმყოფება. მიტოზის ხანგძლივობა დაახლოებით 1სთ-ა, ე. ი. მარცხენა პარკუჭში წელიწადში დაახლოებით 0.71X109 ახალი ბირთვი წარმოიქმნება. რადგანაც 1, 2, და 4-ბირთვიან კარდიომიოციტთა თანაფარდობა 2/1/1-ს შეესაბამება, კარდიომიოციტთა პოტენციურმა ნამატმა წელიწადში შესაძლოა 0,4X109 შეადგინოს. იმავე ავტორთა მონაცემებით, პათოლოგიური გულის (კარდიომიოპათია) მიტოზური ინდექსი, ნორმალურ მიოკარდიუმთან შედარებით 10-ჯერ მეტია. ავტორთა აზრით კარდიომიოციტების პროლიფერაცია მნიშვნელოვან როლს თამაშობს პათოლოგიური მიოკარდიუმის კომპენსატორულ-აღდგენით პროცესებში. მართალია, გამოვლენილი ნამატი ვერ ახდენს მიოკარდიუმის ინფარქტის შემთხვევაში კარდიომიოციტების მასიურ ნეკროზის კომპენსირებას (რადგან ნაწიბუროვანი ქსოვილი უფრო სწრაფად ავსებს დეფექტს), მაგრამ კარდიომიოციტების პროლიფერაციას შეუძლია შექმნას გულის კუნთის გარკვეული რეგენერაციული რეზერვი. უკანასკნელ წლებში გულის კუნთის რეგენერაციის მისაღწევად ახალი მიმართულებები და მიდგომები გამოიკვეთა. ბიოტექნოლოგიების, მოლეკულური და უჯრედული ბიოლოგიის განვითარებამ, უჯრედი არა მარტო ზემოქმედების მთავარ ობიექტად არარმედ მრავალი დაავადების სამკურნალო საშუალებად აქცია [12,13,14] მიაჩნიათ, რომ მიოკარდის ფუნქციის აღდგენა შესაძლებელია მიღწეულ იქნას კუმშვადი ელემენტების რაოდენობის გაზრდის გზით და/ან რეციპიენტის კარდიომიოციტების ფუნქციური რეზერვის გაზრდით, მათში უჯრედული და უჯრედშიდა რეგენერაციის პროცესების სტიმულირების შედეგად. ამ მიზნის მისაღწევად იყენებენ მიოკარდიუმში კარდიომიოციტების, გლუვკუნთოვანი უჯრედების, გენ-მოდიფიცირებული უჯრედების (ფიბრობლასტები, ჩონჩხის მიობლასტები), ძვლის ტვინის ღეროვანი უჯრედების, ემბრიონალური ღეროვანი უჯრედების და სხვ. იმპლანტაციას [15]. ყველა უჯრედული ტექნოლოგია კარდიოლოგიაში გაერთიანებულია ერთი საერთო ტერმინით _ ”უჯრედული კარდიომიოპლასტიკა”. გულის კუნთში უჯრედების გადანერგვას იყენებენ მიოკარდიუმის ინფარქტის შემდეგ ნეკროზული ან ნაწიბუროვანი ქსოვილის კუმშვადი უჯრედებით ჩასანაცვლებლად, გულის კუმშვადი ფუნქციის გასაუმჯობესებლად, რემოდელირების პროცესების დასარეგულირებლად, ანგიოგენეზის სტიმულირების მიზნით და სხვ. შესაძლოა ტრანსპლანტაციის ალტერნატიულ მეთოდად ძვლის ტვინში ღეროვანი უჯრედების წარმოქმნის სტიმულაცია და მისი სისტემურ სისხლის მიმოქცევაში გადასროლა მოგვევლინოს. ამ მიზნით გამოყენებული პრეპარატების ჯგუფიდან აღსანიშნავია კოლონიემასტიმულირებელი ფაქტორები: გრანულოციტური კოლონიემასტიმულირებელი ფაქტორი და გრანულოციტურ-მაკროფაგალური კოლონიემასტიმულირებელი ფაქტორი. Orlik. D. et. al. (2001) მიერ ნაჩვენები იქნა, რომ ვირთაგვებში ექსპერიმენტული მიოკარდიუმის ინფარქტის შემდეგ გრანულოციტური კოლონიემასტიმულირებელი ფაქტორის კანქვეშა შეყვანა იწვევს ინფარქტის ზონაში ახალი კარდიომიოციტების გაჩენას, ჰემოდინამიკური მაჩვენებლების გაუმჯობესებას და ცხოველების სიცოცხლის ხანგძლივობის გაზრდას. ზოგიერთი ავტორის მიერ გამახვილებულია ყურადღება გულის უკმარისობის განვითარებაში მანკიერი წრის როლის შესახებ (მ. როგავა, 2002) [16]. ამ კუთხით ღეროვანი უჯრედების მობილიზაცია და სისხლში მათი რაოდენობის მნიშვნელოვანი გაზრდა ახალ ინტერესს იძენს, რადგანაც არაჰემოპოეზურ ღეროვან უჯრედებს შესწევთ უნარი ჩაენაცვლონ არა მარტო გულის, არამედ მანკიერ წრეში მონაწილე სხვა ორგანოების დაზიანებულ ქსოვილებსაც. კლინიკურ პრაქტიკაში მეცნიერთა ჯგუფის მიერ (Ю. Н. Беленков и соавт. 2003) 5 პაციენტზე განხორციელებულ იქნა იშემიური გენეზის გულის უკმისობის მკურნალობა გრანულოციტური კოლონიემასტიმულირებელი ფაქტორით. მათ შორის ერთ პაციენტში, რომელშიც მიღწეულ იქნა ყველაზე მეტი ღეროვანი უჯრედის მობილიზაცია და სისხლში გადასროლა, აღინიშნა კლინიკური მდგომარეობისა და ექოსკოპიური მონაცემების საგრძნობი გაუმჯობესება [17]. გამომდინარე ზემოთქმულიდან სისტემურ სისხლის მიმოქცევაში ღეროვანი უჯრედების რაოდენობრივი მაჩვენებლების შესწავლა და მისი გაზრდის სამკურნალო ეფექტების დადგენა ძალიან მნიშვნელოვანია არაინვაზიურობისა და შედარებით დაბალი ღირებულების გამო. პერიფერიულ სისხლში ღეროვანი უჯრედებისა და პროგენიტორების რაოდენობრივი მაჩვენებლების კავშირის განსაზღვრა გულის უკმარისობის არსებობასთან და მის სიმძიმესთან დიდ ინტერესს იძენს. კვლევის დიზაინი: კვლევის მიზანს შეადგენდა სხვადასხვა გენეზის გულის უკმარისობის სინდრომით შეპყრობილ პაციენტთა პერიფერიული სისხლის ცოცხალ, ბირთვიან უჯრედებში, ღეროვანი უჯრედების, პროგენიტორებისა და ერითროიდული ხაზის ახალგაზრდა ფორმების პროცენტული შემცველობის განსაზღვრა. ჩვენ მიერ გამოკვლეულ იქნა სხვადასხვა გენეზის გულის ქრონიკული უკმარისობით დაავდებული 110 და ქრონიკული ჰეპატიტით დაავადებული 47 პაციენტი. მათ შორის (127 მამაკაცი და 30 ქალი), ასაკით 19 დან 65 წლამდე (საშ. ასაკი 41±3.7წ.), რომლებიც გადიოდნენ ამბულატორულ და სტაციონარულ მკურნალობას თერაპიის ეროვნულ ცენტრში 2002-2005 წლებში. პაციენტებს კვლევაში მონაწილეობას ვთავაზობდით წერილობითი ფორმით, ჩასატარებელი კვლევის დეტალური აღწერილობითა და მოსალოდნელი შედეგების მითითებით, საქართველოს კანონის “ჯანმრთელობის დაცვის შესახებ” მოთხოვნებისა და სამედიცინო ეთიკის აღიარებული პრინციპების შესაბამისად.
დადებითი სასელექციო კრიტერიუმები
პაციენტის თანხმობა კვლევაში მონაწილეობაზე პაციენტები გულის უკმარისობის სინდრომით (I-IVფ.კ. NYHA), რომელიც გამოწვეულია მიოკარდიუმის კეროვანი ან დიფუზური დაზიანებით (გულის იშემიური დაავადება-პოსტინფარქტული კარდიოსკლეროზი, კარდიომიოპათია). პაციენტები ქრონიკული, არააქტიური ვირუსული ჰეპატიტებით, (B,ჩ,) რომლებსაც მოცემულ მომენტში არ აღენიშნებათ გულის უკმარისობის დამადასტურებელი ჩივილები და კლინიკო-დიაგნოსტიკური ნიშნები. ჯანმრთელი მოხალისეები (საკონტროლო ჯგუფი), რომლებსაც კვლევაში ჩართვის მომენტისათვის თავს გრძნობენ პრაქტიკულად ჯანმრთელად, არ აღენიშნებათ ორგანიზმში მიმდინარე რაიმე პათოლოგიის დამადასტურებელი ობიექტური ნიშნები და შეესაბამებოდნენ შედარების ჯგუფებს დემოგრაფიული მახასიათებლებით (ასაკი, სქესი, შემოსავალი). უარყოფითი სასელექციო კრიტერიუმები · გულის უკმარისობის სინდრომი, გამოწვეული მეორადად რომელიმე ორგანოს პათოლოგიით (თირკმლის უკმარისობა, ფილტვისმიერი გული და სხვ.) · ორგანიზმში მიმდინარე მწვავე ანთებითი პროცესის დამადასტურებელი კლინიკური თუ ლაბორატორიული მონაცემები (ფიბრინოგენის კონცენტრაცია, C რეაქტიული ცილა, ლეიკოციტური ფორმულა, ედს-ი) · სისხლმბადი სისტემის პათოლოგია. · პაციენტის უარი კვლევაში მონაწილეობაზე. აღნიშნული კრიტერიუმების დაკმაყოფილება შეძლო მხოლოდ 108 ავადმყოფმა (მათ შორის 72 პაციენტი გულის უკმარისობით, 36 პაციენტი ქრონიკული არააქტიური ჰეპატიტით) და 31-მა ჯანმრთელმა მოხალისემ. დანარჩენი პაციენტი გამოეთიშა კვლევას სხვადასხვა მიზეზით. კერძოდ 22 მათგანი გამოეთიშა კვლევას საკუთარი სურვილით. 21 პაციენტს აღმოაჩნდა მწვავე ანთებითი პროცესის დამადასტურებელი კლინიკური და ლაბორატორიული მონაცემები. 4 პაციენტს დაუდგინდა ფილტვისმიერი გულის დიაგნოზი. 2 პაციენტის გულის უკმარისობის მიზეზს თირკმლების ქრონიკული უკმარისობა წარმოადგენდა. პაციენტები დაყოფილ იქნა სამ ჯგუფად: I ჯგუფი შეადგინეს პაციენტებმა გულის ქრონიკული უკმარისობით. (n=72) I-IV ფ.კ. (NYHA) (ვირუსული ეტიოლოგიის დილატაციური კარდიომიოპათია, გულის იშემიური დაავადება), მათ შორის 56 (77%) კაცი და 16 (23%) ქალი ასაკით 19 დან 65 წლამდე (საშუალო ასაკი 45.2±9.3წ). I ჯგუფის პაციენტებიდან 35-ის (48.6%) დიაგნოზი იყო დილატაციური კარდიომიოპათია (ვირუსული ეტიოლოგიის: კოკსაკი B3 n=21, ადენოვირუსი n=6, ებშტეინ-ბარის ვირუსი n=7, ჰერპესის ვირუსი n=1). 37-ის (51.4%) გულის იშემიური დაავადება, პოსტინფარქტული კარდიოსკლეროზი. I ჯგუფის პაციენტების ექოსკოპიური და რენტგენოლოგიური გამოკვლევებით გამოვლინდა გულის საზღვრების გადიდება, განდევნის ფრაქცია 48%-დან 20%-მდე. (საშუალოდ 35%±4,1%). პაციენტებში პოსტინფარქტული კარდიოსკლეროზით, ყველა შემთხვევაში კარდიოგრამაზე რეგისტრირდებოდა Q კბილი. 17 (23.6%) შემთხვევაში პოსტინფარქტულ დისფუნქციას ერთვოდა დაძაბვის სტენოკარდია I-III ფ.კ. 5 პაციენტს (6.9%) ჰქონდა შაქრიანი დიაბეტი მე-2 ტიპის. 25 პაციენტს (34.7%) აღენიშნებოდა პარკუჭოვანი ექსტრასისტოლები II-IV გრადაციის Lown-ის მიხედვით. 2-ს (2.7%) პარკუჭოვანი ტაქიკარდიის ეპიზოდები. 4 პაციენტს (5.5%) ჩატარებული ჰქონდა ბალონური ანგიოპლასტიკა. I ჯგუფის პაციენტების გულის უკმარისობის ხანგძლივობა იყო 3 თვიდან 6 წლამდე (საშ. 1.9±0.9წ.). II ჯგუფი Hშეადგინეს პაციენტებმა ქრონიკული ვირუსული ჰეპატიტებით (B , C) (n=36). მათ შორის 29 (80.5%) კაცი და 7 (19.44%) ქალი ასაკით 25 დან 51 წლამდე (საშუალო ასაკი 36±8.3წ). 17 (47.22%) პაციენტი დიაგნოზით ქრონიკული ჰეპატიტი C, 10 (27.7%) პაციენტი ჰეპატიტი B, 7 (19.44%) პაციენტი B და C ჰეპატიტით, 2 (5.55%) პაციენტი ღვიძლის ციროზით (ვირუსული ეტიოლოგიის, C)_Child-Pugh-s მიხედვით A კლასის (კომპენსირებული) დანართი #3. II ჯგუფის პაციენტებს გამოკვლევის მომენტისათვის არ ჰქონდათ ჩივილები გულ-სისხლძარღვთა სისტემის მხრივ, ექოსკოპიური და რენტგენოლოგიური გამოკვლევებით არ აღენიშნებოდათ გულის საზღვრების გაზრდა, განდევნის ფრაქცია არ იყო 55%-ზე დაბალი (საშ. 57±1.7%). II ჯგუფის პაციენტების დაავადების ხანგძლივობა იყო 1 დან 7 წლამდე (საშ. 3±1.9წ.). III ჯგუფი შეადგინეს ჯანმრთელმა მოხალისეებმა (n=31), რომლებიც კვლევაში ჩართვის მომენტისათვის თავს გრძნობდნენ პრაქტიკულად ჯანმრთელად და არ აღენიშნებოდათ ორგანიზმში მიმდინარე რაიმე პათოლოგიის დამადასტურებელი ობიექტური ნიშნები. მათ შორის 26 (8.87%) კაცი და 5 (16.13%) ქალი ასაკით 22 დან 59 წლამდე (საშუალო ასაკი 43±7.8წ). ექოსკოპიური და რენტგენოლოგიური გამოკვლევებით არ აღენიშნებოდათ გულის საზღვრების გაზრდა, განდევნის ფრაქცია არ იყო 55%-ზე დაბალი (საშ. 60±3.1%). სისხლის ვირუსოლოგიური კვლევით არ გამოუვლინდათ HbsAg, anti-HBV, anti-HCV. ALT არ იყო აწეული. I ჯგუფის პაციენტებს (გულის უკმარისობა) არამედიკამენტოზური მკურნალობის ფონზე უტარდებოდათ მკურნალობა აგფ-ინჰიბიტორებით, შარდმდენებით, ß- ბლოკატორებით, ალდოსტერონის ინჰიბიტორებით, პერიფერიული ვაზოდილატატორებით, დიგიტალისით, ევროპის კარდიოლოგთა ასოციაციის მიერ მოწოდებული კრიტერიუმების გათვალისწინებით. II ჯგუფის პაციენტებს არამედიკამენტოზური მკურნალობის ფონზე უტარდებოდათ მკურნალობა ინტერფერონებით, ჰეპატოპროტექტორებით. I ჯგუფი დაყოფილ იქნა ორ ქვეჯგუფად. Iა ქვეჯგუფი შეადგინეს პაციენტებმა გულის უკმარისობით I-II ფ.კ. n=32 (NYHA) მათ შორის 26 (81.25%) კაცი და 6 (28.75%) ქალი ასაკით 39 დან 59 წლამდე (საშუალო ასაკი 49.3±7.8წ) და Iბ ქვეჯგუფი პაციენტებმა გულის უკმარისობით III-IV ფ.კ. (NYHA) n=40. მათ შორის 30 (75%) კაცი და 10 (25%) ქალი ასაკით 19 დან 58 წლამდე (საშუალო ასაკი 36.1±9.1წ). სტაციონარში ხდებოდა ავადმყოფების ანამნეზის შეგროვება, ჩივილების შეფასება, ელექტროკარდიოგრაფიული, ექოკარდიოსკოპიული, რენტგენოგრაფიული, სისხლის კლინიკო-დიაგნოსტიკური, ბიოქიმიური კვლევები. გულის უკმარისობის დიაგნოზს ვსვამდით ევროპის კარდიოლოგთა ასოციაციის მიერ მოწოდებული რეკომენდაციების გათვალისწინებით. ავადმყოფთა გულის უკმარისობის ფუნქციურ კლასს ვადგენდით ამერიკის გულის ასოციაციის მიერ მოწოდებული კრიტერიუმებით. გარდა რუტინული კვლევებისა ხდებოდა ავადმყოფთა პერიფერიულ სისხლში ღეროვანი და პროგენიტორული უჯრედებისა და ერითროიდული ხაზის ახალგაზრდა ფორმების შემცველობის განსაზღვრა. პერიფერიულ სისხლში უჯრედების იმუნოფენოტიპირებას ვახდენდით გამდინარე ციტომეტრიის საშუალებით, მონოკლონარული ანტისხეულებით მონიშვნის გზით. ავადმყოფთა ერთ ნაწილს ასეთი კვლევა უტარდებოდა განმეორებით კლინიკური მდგომარეობის გაუმჯობესების შემდეგ. კვლევა ატარებდა ორმაგი ბრმა ობსერვაციული კვლევის ხასიათს. კვლევაში მონაწილეობდა 3 პირი. ლაბორანტი და მონაცემების დამმუშავებელი ოპერატორი, რომლებსაც არ ჰქონდათ ინფორმაცია კვლევის მიზანის, მოსალოდნელი შედეგებისა და კვლევაში მონაწილე პაციენტების შესახებ. მესამე პირი “ოქროს სტანდარტის” (ამერიკის გულის ასოციაციის მიერ მოწოდებული კრიტერიუმები NYHA) საფუძველზე აფასებდა დაავადებას და არ ფლობდა იმფორმაციას პერიფერიული სისხლის იმუნოფენოტიპირების შედეგების შესახებ. პერიფერიული სისხლის იმუნოფენოტიპირება: (CD34+, CD133+CD34- უჯრედები) და ერითროიდული ხაზის ახალგაზრდა უჯრედების (GP-A+ უჯრედები) რაოდენობრივ შესწავლას. ჩატარებული კვლევა ითვალისწინებდა პერიფერიულ სისხლის ცოცხალ ბირთვიან უჯრედებში ღეროვანი უჯრედების, პროგენიტორებისა. CD34- წარმოადგენს ტრანსმემბრანულ გლიკოპროტეინს, რომელიც ექსპრესირდება ჰემოპოეზურ ღეროვან უჯრედებსა და პროგენიტორებზე. უკანასკნელი ათწლეულის განმავლობაში ის გამოიყენებოდა ჰემოპოეზური ღეროვანი უჯრედებისა და პროგენიტორების აღმომჩენ მარკერად. CD133 ღეროვანი უჯრედებისა და პროგენიტორების ახალი მარკერია. CD133 ტრანსმემბრანული გლიკოპროტეინია [18,19,20,21]. CD133 ექსპრესირდება არამწიფე ღეროვან უჯრედზე და პროგენიტორებზე. CD34 ისაგან განსხვავებით ის არ აღინიშნება ბოლო რიგის პროგენიტორებზე (მაგ. პრე B უჯრედები, CFU-E, და CFU-G). CD133- ის აღმომჩენი ანტისხეულები ღებავენ CD34 უჯრედების 35-75%-ს, მათ შორის (CD34bright, CD38neg/dim, HLA-DR-, CD90+ და CD117+) უჯრედებს (ანუ CD34 პოზიტიური უჯრედების 35-75% CD133_პოზიტიურია). ამასთან ერთად იდენტიფიცირებულია CD34-CD133+ უჯრედების გარკვეული რაოდენობა [22,23,24,25]. ბოლო წლების კვლევებმა აჩვენა, რომ CD133+CD34- უჯრედები გვევლინება როგორც არაჰემოპოეზური სისტემის ღეროვანი უჯრედებისა და პროგენიტორების მარკერი. მაგ. (ნერვული ღეროვანი უჯრედი, ემბრიონარული ღეროვანი უჯრედი და ზრდასრული ადამიანის ორგანიზმის პლურიპოტენტური ღეროვანი უჯრედები. ყველა ეს უჯრედი CD34 ნეგატიურია [26,27,28,]. ნაჩვენები იქნა, რომ CD133+CD34- უჯრედებს გააჩნიათ ვირთაგვის ექტოდერმალური, მეზოდერმალური და ენდოდერმალური წარმოშობის ორგანოებში მიგრირების (მაგ. თავის ტვინის, განივზოლიანი კუნთის, გულის, ნაწლავის, ფილტვის, ღვიძლის) და დიფერენცირების უნარი [29]. აგრეთვე ინ ვივო კვლევებში ნაჩვენები იქნა, რომ CD133+ უჯრედებს გააჩნიათ ენდოთელიალურ უჯრედებად დიფერენცირების უნარი, ამდენად მათ გამოყენება ჰპოვეს ანგიოგენეზის სტიმულირებაში მიოკარდიუმის ინფარქტის შემდეგ [30,31,32]. სიალისმჟავის გლიკოპროტეინები (გლიკოფორინი A, B, C, D, E) შეადგენენ ინტეგრალური პროტეინებად წოდებული გლიკოფორინების კლასს, რომლებიც წითელი უჯრედების მემბრანის პროტეინების დაახლოებით 2%-ს შეადგენენ. GP-A- ს შეაქვს წვლილი ზოგიერთი ვირუსისა და პარაზიტების ინვაზიასა და ზრდაში (მაგ: გრიპის ვირუსი, მალარია Plasmodium falciparum) [33,34]. მიაჩნიათ, რომ გლიკოფორინი ქმნის კომპლექსს ერითროციტის მემბრანის სხვა კომპონენტებთან (ანკირინი, band-3, პროტეინი 4.2) [35] და მათი ასოციაცია განაპირობებს წითელი უჯრედების მემბრანების მექანიკურ თვისებებს [36,37,38,39]. უკანასკნელი წლების კვლევებში GP-A- ს გამოიყენებენ, როგორც ერითროიდული ხაზის უჯრედების აღმომჩენ მარკერს. ჩვენს კვლევაში გამდინარე ციტომეტრიის საშუალებით ვიკვლევდით მხოლოდ ბირთვიან უჯრედებს, უბირთვო უჯრედები (მათ შორის ერითროციტები) წინასწარ იშლებოდა სპეციალური მეთოდიკით. ე.ი. ჩვენს მიერ გამოკვლეული GP-A უჯრედები. წარმოადგენდნენ ერითროიდულ პრეკურსორებს (ერითროიდული ხაზის ახალგაზრდა ფორმები). CD (CD34, CD133, CD253) მარკერების შესწავლა ხდებოდა: Becton&Dickinson-ის (აშშ) გამდინარე ციტომეტრის მეშვეობით ჩვენს მიერ აღწერილი მეთოდიკით (ჟურნ. “კარდიოლოგია და შინაგანი მედიცინა”, 2005 წ. #2). მონაცემთა სტატისტიკურად მუშავდებოდა კომპიუტერული პროგრამის SPSS- ის საშუალებით. მაჩვენებლების განაწილების კანონი განსხვავდებოდა ნორმალური განაწილებისაგან და განსხვავება ჯგუფებს შორის ისაზღვრებოდა მანნა-უიტნის U კრიტერიუმით (არაპარამეტრული მეთოდი). პაციენტების ჯგუფებში მკურნალობამდე და მკურნალობის შემდეგ განსხვავებას ვადგენდით უილკოკსონის t კრიტერიუმით დამოკიდებული ცვლადებისათვის. განსხვავება ჯგუფებს შორის სტატისტიკურად სარწმუნოდ ითვლებოდა თუ P<0.05.
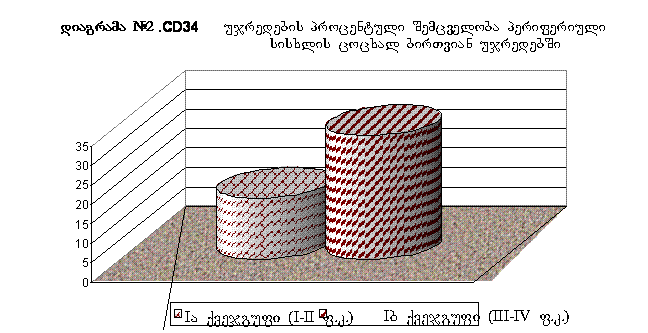
მიღებული შედეგები: ჩატარებული კვლევის შედეგები მოყვანილია ცხრილებისა და დიაგრამების სახით. (ცხრლი #1-2, დიაგრამა #1-2) სადაც მაჩვენებლები მოყვანილია როგორც საშუალო არითმეტიკული ± სტანდარტული გადახრა. მიღებული შედეგების დამუშავების შედეგად გამოვლინდა სტატისტიკურად სარწმუნო განსხვავება I (გულის უკმარისობა) და III (ჯანმრთელი მოხალისეები) ჯგუფებს შორის CD34 ujredebis procentuli Semcvelobis mixedviT (p=0.002). ეს მაჩვენებელი უფრო მაღალი აღმოჩნდა პაციენტების ჯგუფში გულის უკმარისობით, ჯანმრთელი მოხალისეების ჯგუფთან შედარებით (I ჯგუფი _ 24.15±6.15%, III_ჯგუფი 0.24±0.18%). აგრეთვე გამოვლინდა სტატისტიკურად სარწმუნო განსხვავება II (ქრონიკული ჰეპატიტი) და III (ჯანმრთელი მოხალისეები) ჯგუფებს შორისაც. CD34 უჯრედების პროცენტული შემცველობის მიხედვით (p=0.001). საშუალო მნიშვნელობების მიხედვით CD34 დადებითი უჯრედების უფრო მაღალი შემცველობა გამოვლინდა პაციენტების ჯგუფში ვირუსული ჰეპატიტებით ჯანმრთელი მოხალისეების ჯგუფთან შედარებით (II ჯგუფი_26.55±7.68%, III ჯგუფი _ 0.24±0.18%). ვერ გამოვლინდა სტატისტიკურად სარწმუნო განსხვავება პაციენტების I (გულის უკმარისობა) და II (ქრონიკული ჰეპატიტი) ჯგუფებს შორის CD34 უჯრედების პროცენტული შემცველობის მიხედვით (p=0.54). გამოვლინდა სტატისტიკურად სარწმუნო განსხვავება Iა (I-II ფ.კ. NYHA) და Iბ (III-IV ფ.კ. NYHA) ქვეჯგუფებს შორის შორის CD34 უჯრედების პროცენტული შემცველობის მიხედვით (p<0.05). საშუალო მნიშვნელობების მიხედვით CD34 დადებითი უჯრედების უფრო დაბალი შემცველობა გამოვლინდა პაციენტების ჯგუფში გულის უკმარისობის უფრო მსუბუქი ხარისხით მძიმე უკმარისობის ჯგუფთან შედარებით (Iა ქვეჯგუფი_15.75±9.13%, Iბ ქვეჯგუფი_32.0±8.9%).
ცხრილი #1. CD34+ უჯრედების, პროცენტული შემცველობა პერიფერიული სისხლის ცოცხალ, ბირთვიან უჯრედებში. I ჯგუფი_პაციენტები გულის უკმარისობის სინდრომით (I-IV ფ.კ. NYHA), II ჯგუფი_პაციენტები ქრონიკული ჰეპატიტით, III ჯგუფი_ჯანმრთელი მოხალისეები.
ცხრილი #2. CD34+ უჯრედების, პროცენტული შემცველობა პერიფერიული სისხლის ცოცხალ, ბირთვიან უჯრედებში. Iა ქვეჯგუფი_პაციენტები გულის უკმარისობის სინდრომით (I-II ფ.კ. NYHA), Iბ ქვეჯგუფი_პაციენტები გულის უკმარისობის სინდრომით (III-IV ფ.კ. NYHA).
CD133+ CD34- უჯრედების პროცენტული შემცველობა პერიფერიული სისხლის ცოცხალ, ბირთვიან უჯრედებში: ჩატარებული კვლევის შედეგები მოყვანილია ცხრილებისა და დიაგრამების სახით. (ცხრლი #3-4, დიაგრამა #3-4) მიღებული შედეგების დამუშავების შედეგად ვერ გამოვლინდა სტატისტიკურად სარწმუნო განსხვავება I (გულის უკმარისობა) და III (ჯანმრთელი მოხალისეები) ჯგუფებს შორის CD133+CD34- უჯრედების პროცენტული შემცველობის მიხედვით (p=0.47). აღნიშნულ ჯგუფებში გამოვლინდა ამ მაჩვენებელის შემდეგი საშუალო მნიშვნელობები_(I ჯგუფი_1.83±0.9%, III_ჯგუფი 0.84±0.46%). აგრეთვე ვერ გამოვლინდა სტატისტიკურად სარწმუნო განსხვავება II (ქრონიკული ჰეპატიტი) და III (ჯანმრთელი მოხალისეები) ჯგუფებს შორისაც. CD133+CD34- უჯრედების პროცენტული შემცველობის მიხედვით (p=0.77). აღნიშნულ ჯგუფებში გამოვლინდა ამ მაჩვენებელის შემდეგი საშუალო მნიშვნელობები (II ჯგუფი_1.24±0.48%, III_ჯგუფი 0.84±0.46%). ვერ გამოვლინდა სტატისტიკურად სარწმუნო განსხვავება პაციენტების I (გულის უკმარისობა) და II (ქრონიკული ჰეპატიტი) ჯგუფებს შორის CD34 უჯრედების პროცენტული შემცველობის მიხედვით (p=0.47). განსხვავება Iა (I-II ფ.კ. NYHA) და Iბ (III-IV ფ.კ. NYHA) ქვეჯგუფებს შორის შორის CD133+CD34- უჯრედების პროცენტული შემცველობის მიხედვით აგრეთვე არ ატარებდა სტატისტიკურად სარწმუნო ხასიათს (p=0.27). საშუალო მნიშვნელობების მიხედვით CD34 დადებითი უჯრედების უფრო დაბალი შემცველობა გამოვლინდა პაციენტების ჯგუფში გულის უკმარისობის უფრო მსუბუქი ხარისხით, მძიმე უკმარისობის ჯგუფთან შედარებით (Iა ქვეჯგუფი_1.81±1.14%, Iბ ქვეჯგუფი_2.06±1.85%). ცხრილი #3. CD34-CD133+ უჯრედების, პროცენტული შემცველობა პერიფერიული სისხლის ცოცხალ ბირთვიან უჯრედებში. I ჯგუფი_პაციენტები გულის უკმარისობის სინდრომით (I-IV ფ.კ. NYHA), II ჯგუფი_პაციენტები ქრონიკული ჰეპატიტით, III ჯგუფი ჯანმრთელი მოხალისეები
ცხრილი #4. CD133+CD34- უჯრედების, პროცენტული შემცველობა პერიფერიული სისხლის ცოცხალ ბირთვიან უჯრედებში. Iა ქვეჯგუფი_პაციენტები გულის უკმარისობის სინდრომით (I-II ფ.კ. NYHA), Iბ ქვეჯგუფი_პაციენტები გულის უკმარისობის სინდრომით (III-IV ფ.კ. NYHA)
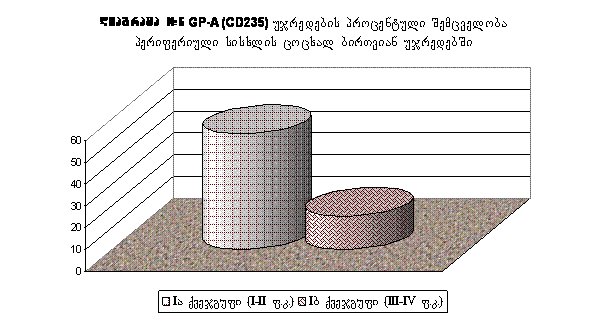
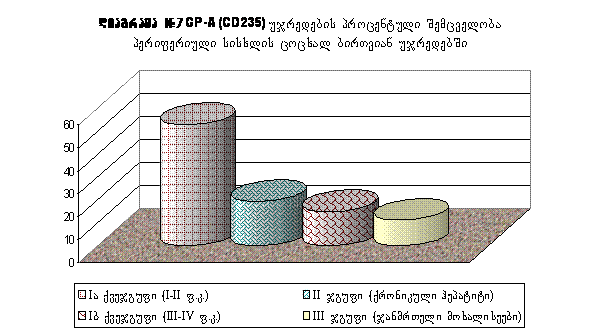
GP-A (CD235) + უჯრედების პროცენტული შემცველობა პერიფერიული სისხლის ცოცხალ, ბირთვიან უჯრედებში: ჩატარებული კვლევის შედეგები მოყვანილია ცხრილებისა და დიაგრამების სახით. (ცხრლი #5-6, დიაგრამა #5-7). მიღებული შედეგების დამუშავების შედეგად ვერ გამოვლინდა სტატისტიკურად სარწმუნო განსხვავება I (გულის უკმარისობა) და III (ჯანმრთელი მოხალისეები) ჯგუფებს შორის GP-A უჯრედების პროცენტული შემცველობის მიხედვით (p=0.2). აღნიშნულ ჯგუფებში გამოვლინდა ამ მაჩვენებელის შემდეგი საშუალო მნიშვნელობები_(I ჯგუფი_23.44±7.11%, III_ჯგუფი 11.4±8.43%). აგრეთვე ვერ გამოვლინდა სტატისტიკურად სარწმუნო განსხვავება II (ქრონიკული ჰეპატიტი) და III (ჯანმრთელი მოხალისეები) ჯგუფებს შორისაც. GP-A უჯრედების პროცენტული შემცველობის მიხედვით (p=0.23). აღნიშნულ ჯგუფებში გამოვლინდა ამ მაჩვენებელის შემდეგი საშუალო მნიშვნელობები_(II ჯგუფი_19.4±4.44%, III_ჯგუფი 11.4±8.43%). ვერ გამოვლინდა სტატისტიკურად სარწმუნო განსხვავება პაციენტების I (გულის უკმარისობა) და II (ქრონიკული ჰეპატიტი) ჯგუფებს შორის GP-A უჯრედების პროცენტული შემცველობის მიხედვით (p=0.64). განსხვავება Iა (I-II ფ.კ. NYHA) და Iბ (III-IV ფ.კ. NYHA) ქვეჯგუფებს შორის შორის GP-A უჯრედების პროცენტული შემცველობის მიხედვით ატარებდა სტატისტიკურად სარწმუნო ხასიათს (p<0.01). საშუალო მნიშვნელობების მიხედვით GP-A დადებითი უჯრედების უფრო მაღალი შემცველობა გამოვლინდა პაციენტების ჯგუფში გულის უკმარისობის უფრო მსუბუქი ხარისხით, მძიმე უკმარისობის ჯგუფთან შედარებით (Iა ქვეჯგუფი_53.1±10.26%, Iბ ქვეჯგუფი_15.08±5.44%). გამოვლინდა სტატიკურად სარწმუნო განსხვავება (p<0.01) Iა ქვეჯგუფსა (გულის უკმარისობა I-II ფ.კ. NYHA) და III ჯგუფს შორის (ჯანმრთელი მოხალისეები). ეს მაჩვენებელი უფრო მაღალი აღმოჩნდა პაციენტების ჯგუფში გულის უკმარისობის I-II ფუნქციონალური კლასით (NYHA), ჯანმრთელი მოხალისეების ჯგუფთან შედარებით (Iა ქვეჯგუფი_53.1±10.26%, III_ჯგუფი 11.4±8.43%). აგრეთვე გამოვლინდა სტატისტიკურად სარწმუნო განსხვავება (p<0.01) Iა ქვეჯგუფსა (გულის უკმარისობა I-II ფ.კ. NYHA) და II ჯგუფს შორის (ქრონიკული ჰეპატიტი). ეს მაჩვენებელი უფრო მაღალი აღმოჩნდა პაციენტების ჯგუფში გულის უკმარისობის I-II ფუნქციონალური კლასით NYHA, ქრონიკული ჰეპატიტის ჯგუფთან შედარებით (Iა ქვეჯგუფი_53.1±10.26%, II_ჯგუფი 19.4±4.44%). ცხრილი #5. GP-A (CD235)+ უჯრედების, პროცენტული შემცველობა პერიფერიული სისხლის ცოცხალ ბირთვიან უჯრედებში. I ჯგუფი_პაციენტები გულის უკმარისობის სინდრომით (I-IV ფ.კ. NYHA), II ჯგუფი_პაციენტები ქრონიკული ჰეპატიტით, III ჯგუფი ჯანმრთელი მოხალისეები
ცხრილი #6. GP-A+(CD235) უჯრედების პროცენტული შემცველობა პერიფერიული სისხლის ცოცხალ ბირთვიან უჯრედებში. Iა ქვეჯგუფი პაციენტები გულის უკმარისობის სინდრომით (I-II ფ.კ.), Iბ ქვეჯგუფი პაციენტები გულის უკმარისობის სინდრომით (III-IV ფ.კ).

CD34, CD34-CD133+ უჯრედების პროცენტული შემცველობა პერიფერიული სისხლის ცოცხალ ბირთვიან უჯრედებში პაციენტებში მკურნალობამდე და მკურნალობის შემდეგ: 21 პაციენტი გულის უკმარისობის სინდრომით (მათ შორის 10 პაციენტი III-IV ფ.კ. და 11 პაციენტი I_IIფ.კ. NYHA) გამოკვლეულ იქნა ზედაპირულ ანტიგენებზე განმეორებით. ჩატარებული კვლევის შედეგად მიღებული შედეგები მოყვანილია ცხრილებისა და დიაგრამების სახით. (ცხრლი #7, დიაგრამა #13-14) სადაც მაჩვენებლები მოყვანილია როგორც საშუალო არითმეტიკული ± სტანდარტული გადახრა Mean±St. Dev მიღებული შედეგების დამუშავების შედეგად გამოვლინდა სტატისტიკურად სარწმუნო განსხვავება მაჩვენებლებს შორის მკურნალობამდე და მკურნალობის შემდეგ CD34 და CD34-CD133+ უჯრედების მიხედვით (p<0,05) და (p<0.05) შესაბამისად. ეს მაჩვენებლები უფრო მაღალი აღმოჩნდა პაციენტებში მკურნალობამდე, ანუ მაშინ როდესაც მათი მდგომარეობა ფასდებოდა გულის უკმარისობის უფრო მაღალი ფუნქციური კლასით. ცხრილი #7. CD34, CD133+CD34- უჯრედების, პროცენტული შემცველობა პერიფერიული სისხლის ცოცხალ ბირთვიან უჯრედებში პაციენტებში მკურნალობამდე და მკურნალობის შემდეგ n=21
მიღებული შედეგების განხილვა: როგორც ჩატარებული კვლევის შედეგებმა აჩვენა, გულის უკმარისობისას ადგილი აქვს პერიფერიულ სისხლში GP-A ბირთვიანი, უჯრედების (ერითროიდული პრეკურსორები) რაოდენობის მნიშვნელოვან ზრდას. ერითროიდული ხაზის ახალგაზრდა ფორმების ასეთ ზრდას (GP-A) ადგილი აქვს მხოლოდ გულის უკმარისობის შედარებით მსუბუქი ფორმების შემთხვევაში_I-II ფ.კ. ხოლო III-IV ფ.კ.-ის გულის უკმარისობის ჩამოყალიბების შემთხვევაში ადგილი აქვს პერიფერიულ სისხლში მათი რაოდენობის მნიშვნელოვან შემცირებას, რაც ჩვენი აზრით მანკიერი წრის პროგრესირებაზე მიუთითებს. (უკანასკნელი წლების ინ ვივო კვლევებში გამოვლინდა, რომ TNF-A გააჩნია ერითროპოეზის ინჰიბირების უნარი [40], შესაძლოა ასეთი უჯრედების რაოდენობის შემცირება გულის უკმარისობის პროგრესირებისას TNF-Aს როგორც ერითროპოეზის უარყოფითი რეგულატორის კონცენტრაციის ზრდასთან იყოს დაკავშირებული). მიგვაჩნია, რომ GP-A შესაძლოა გამოყენებულ იქნას გულის უკმარისობის სადიაგნოსტიკო ტესტად. ამის საფუძველს გვაძლევს GP-A უჯრედების ცვლილებების გამოვლენილი კანონზომიერება გულის უკმარისობის ჩამოყალიბებასთან და მიმდინარეობასთან კავშირში, ასეთი უჯრედების რაოდენობის მკვეთრი ზრდა გულის უკმარისობის ჩამოყალიბებისას და შედარებით მსუბუქი ფორმებისას. აგრეთვე ის, რომ არ გამოვლინდა GP-A უჯრედების სტატისტიკურად სარწმუნო ზრდა ქრონიკული ჰეპატიტებით დაავადებულ პაციენტებში. აღსანიშნავია ის გარემოება, რომ კვლევაში მონაწილეობდნენ პაციენტები გულის უკმარისობის I ფუნქციონალური კლასით, რომელთაც გამოუვლინდათ მიოკარდიუმის დისფუნქცია, მაგრამ მათი მხრიდან გულის უკმარისობის გამოვლინებანი უყურადღებოდ რჩებოდა. ასეთ პაციენტებში გამოვლინდა GP-A უჯრედების მაღალი პროცენტული შემცველობა პერიფერიული სისხლის ცოცხალ, ბირთვიან უჯრედებში. ყოველივე ზემოთქმულიდან შეიძლება დავასკვნათ, რომ აღნიშნული ტესტის გამოყენება შესაძლოა ეფექტური იყოს გულის უკმარისობის სკრინინგისათვის.DAN GAMO ჩვენ მიერ ჩატარებული კვლევის მონაცემების დამუშავების მიხედვით გამოთვლილი იქნა აღნიშნული ტესტის ოპერაციული მახასიათებლები. ოქროს სტანდარტად მიღებულ იქნა ამერიკის გულის ასოციაციის მიერ მოწოდებული კრიტერიუმები გულის უკმარისობის შესაფასებლად, კერძოდ I-II ფუნქციონალური კლასი. კრიტიკულ ზღვარად აღებულ იქნა აღნიშნული უჯრედების 50%. აღნიშნულის გათვალისწინებით გაანგარიშებულ იქნა სადიაგნოსტიკო ტესტის ოპერაციული მახასიათებლები_მგრძნობელობა და სპეციფიურობა. ჩვენი კვლევის შედეგების მიხედვით აღნიშნული ტესტის მგრძნობელობა გულის უკმარისობის I-II ფ.კ. პაციენტების გამოსავლენად შეადგენს 70%-ს. სპეციფიურობა 95%-ს. გამოთვლილ მიქნა ტესტის დადებითი და უარყოფითი მნიშვნელობის პროგნოზული ღირებულება სხვადასხვა პრევალენსის გათვალისწინებით. მონაცემები მოყვანილია ცხრილებში #8,9. ცხრილი #8 ტესტის მგრძნობელობისა და სპეციფიურობის განსაზღვრა
ტესტის ოპერაციული მახასიათებლები მგრძნობელობა დადებითი ტესტის პროგნოზული მნიშვნელობა Sn= სპეციფიურობა უარყოფითი ტესტის პროგნოზული მნიშვნელობა Sp= ცხრილში #9 მოყვანილია დადებითი და უარყოფითი ტესტის პროგნოზული მნიშვნელობები (ბაიესის თეორიის გამოყენებით) მგრძნობელობის და სპეციფიურობის ჩვენ მიერ მიღებული შედეგებისათვის, (მგრძნობელობა 70%, სპეციფიურობა 95%) დაავდების საწყისი ალბათობის (პრევალენსი) გათვალისწინებით. ცხრილი #9 ტესტის პრედიქტორული მნიშვნელობა სპეციფიურობის 95% და მგრძნობელობის 70% მნიშვნელობისას დაავადებათა სხვადასხვა საწყისი ალბათობის დონეზე.
ჩვენს მიერ ჩატარებული კვლევის შედეგებმა გვიჩვენა, რომ გულის უკმარისობის სინდრომისას ადგილი აქვს პერიფერიულ სისხლში ჰემოპოეზური ღეროვანი უჯრედებისა და პროგენიტორების (CD34) რაოდენობრივ ზრდას, საკონტროლო ჯგუფთან (ჯანმრთელი მოხალისეები) შედარებით, კვლევაში გამოვლინდა, რომ აღნიშნული უჯრედების სტატისტიკურად სარწმუნო რაოდენობრივ ზრდას, ასევე ადგილი აქვს ქრონიკული ჰეპატიტებით დაავადებულ პაციენტებშიც. ყოველივე ზემოთქმულიდან გამომდინარე შესაძლოა ვივარაუდოთ, რომ ჰემოპოეზური ღეროვანი უჯრედებისა და პროგენიტორების რაოდენობრივ ზრდას პერიფერიულ სისხლში შესაძლოა ადგილი ჰქონდეს სხვადასხვა პათოლოგიური პროცესების დროს, რაც სხვა კვლევებში უნდა დადასტურდეს. პაციენტების ჯგუფში მკურნალობამდე და მკურნალობის შემდეგ, აღინიშნა CD34 უჯრედების პროცენტული შემცველობის სტატისტიკურად სარწმუნო შემცირება პაციენტებში ეფექტური მკურნალობის შემდეგ, მაშინ როცა მათი მდგომარეოპბა შეფასდა, როგორც გულის უკმარისობის უფრო დაბალი ფუნქციონალური კლასი. რაც შეეხება CD133+CD34- ღეროვან უჯრედებსა და პროგენიტორებს, რომლებსაც დღეისათვის არაჰემოპოეზური სისტემის უჯრედებად მიიჩნევენ (უჯრედები რომელთა პლურიპოტენტური პოტენციალი დამტკიცებულია სხვადასხვა კვლევებში), ჩვენს მიერ ჩატარებულ კვლევაში გამოიკვეთა მათი საშუალო მნიშვნელობის ზრდა გულის უკმარისობითა და ქრონიკული ვირუსული ჰეპატიტით დაავადებულ პაციენტებში საკონტროლო ჯგუთან შედარებით, მაგრამ აღნიშნული ცვლილება არ ატარებდა სტატისტიკურად სარწმუნო ხასიათს. ამასთან ერთად ჩატარებულ კვლევაში პაციენტებში მკურნალობამდე და მკურნალობის შემდეგ აღინიშნა ზემოხსენებული უჯრედების სტატისტიკურად სარწმუნო შემცირება პაციენტებში მკურნალობის შემდეგ, მაშინ როცა მათი მდგომარეობა შეფასდა, როგორც გულის უკმარისობის უფრო დაბალი ფუნქციონალური კლასი. გამომდინარე იქიდან, რომ ჩატარებულ კვლვაში პაციენტების ჯგუფში მკურნალობამდე და მკურნალობის შემდეგ ღეროვანი უჯრედებისა და პროგენიტორების რაოდენობრივი მაჩვენებლის შემცირება პაციენტებში შედეგიანი მკურნალობის შემდეგ გამოხატული იყო თითქმის ყველა შემთხვევაში, მიგვაჩნია, რომ CD34 და CD133+CD34- უჯრედების აღნიშნული რაოდენობრივი ცვლილებები შესაძლოა გამოყენებულ იქნას გულის უკმარისობის მკურნალობის მონიტორინგისათვის. ჩატარებულ კვლევაში გამოიკვეთა, რომ ჯანმრთელი პაციენტების პერიფერიულ სისხლში აღინიშნება CD133+CD34- (არაჰემოპოეზური უჯრედები) უჯრედების უფრო მაღალი შემცველობა, ვიდრე CD34 (ჰემოპოეზური უჯრედები) უჯრედებისა. სხვადასხვა ავტორთა კვლევებში მათი მონაცემების მიხედვით, კი დადგენილია, რომ ძვლის ტვინში CD34 უჯრედების 35-75%-ზე ექსპრესირდება CD113 ანტიგენი, ხოლო CD133+CD34- უჯრედები ძალიან მცირე რაოდენობითაა. მივიჩნევთ, რომ CD133+CD34- უჯრედების უფრო მაღალი დონე CD34 უჯრედებთან შედარებით, როგორც ორგანიზმის “საშენი მასალის”- CD133+CD34- უჯრედების მოთხოვნილებითაა გამოწვეული. ჯანმრთელ ადამიანებში დღეისათვის ჩვენთვის უცნობი მექანიზმები განაპირობებენ ასეთი უჯრედების გადასროლას პერიფერიულ სისხლის მიმოქცევაში. პათოლოგიური პროცესის მიმდინარეობისას. კი მათი რაოდენობა პერიფერიულ სისხლში კიდევ უფრო იზრდება. რაც შეეხება CD34 უჯრედებს მათი რაოდენობა ჯანმრთელი ადამიანების პერიფერიულ სისხლში მინიმალურია, მაგრამ რამოდენიმეჯერ იზრდება პათოლოგიური პროცესის მიმდინარეობისას. ჩატარებული კვლევის შედეგებმა გვიჩვენა, რომ გულის უკმარისობის სინდრომისას ადგილი აქვს პერიფერიულ სისხლში ღეროვანი ჰემოპოეზური უჯრედებისა და პროგენიტორების (CD34) სტატისტიკურად სარწმუნო რაოდენობრივ ზრდას საკონტროლო ჯგუფთან შედარებით. ჩატარებული კვლევის შედეგებმა გვიჩვენა, რომ გულის უკმარისობის სინდრომისას ადგილი აქვს პერიფერიულ სისხლში ღეროვანი არაჰემოპოეზური უჯრედებისა და პროგენიტორების (CD133+CD34-) რაოდენობრივ ზრდას საკონტროლო ჯგუფთან შედარებით (საშუალო მნიშვნელობების მიხედვით), მაგრამ აღნიშნული ცვლილება არ ატარებდა სტატისტიკურად სარწმუნო ხასიათს. პაციენტების ჯგუფში მკურნალობამდე და მკურნალობის შემდეგ ფუნქციური კლასის ცვლილებასთან ერთად, ადგილი აქვს CD34, CD34-CD133+ უჯრედების სტატისტუკურად სარწმუნო რაოდენობრივ ცვლილებებს გულის უკმარისობის სიმძიმის პრალელურად. გამოვლინდა, რომ ჯანმრთელ საკონტროლო ჯგუფის პერიფერიული სისხლის CD133+CD34 უჯრედების (არაჰემოპოეზური ღეროვანი უჯრედები და პროგენიტორები) შემცველობა უფრო მაღალია ვიდრე CD34 უჯრედებისა (ჰემოპოეზური ღეროვანი უჯრედები და პროგენიტორები) CD34/CD133<1. დაავადების შემთხვევაში (ორგანოთა დაზიანებისას) ეს ფარდობა იცვლება საპირისპირო მხარეს CD34/CD133>1. დასკვნის სახით გვინდა ავღნიშნოთ, რომ პერიფერიულ სისხლში CD34, CD133+CD34- და GP-A უჯრედების შემცველობის შესწავლა დიდ ინტერესს იძენს და სამომავლოდ შესაძლოა ამ მაჩვენებლებმა გამოყენება ჰპოვონ კლინიკურ პრაქტიკაში, გულის უკმარისოპბის სკრინინგისა და მონიტორინგისათვის. ლიტერატურა: 1. Lucas RV, Edwards JE. Curr Probl Cardiol 1982; 7: 1-48. 2. Степура О.Б., Мартынов А.И., Остроумова О.Д. Кардиология. 1995; 5: 23-6. 3. Bonow А. et al. JACC 1998; 32 (5): 1525-30. 4. Сторожаков Г.И., Верещагина Г.С. Тер. архив. 1998; 4: 27-32. 5. Zuppiroli A, Rinaldi M, Kramer R. et al. Am J Card 1995; 75: 1028-32. 6. Сторожаков Г.И., Верещагина Г.С., Малышева Н.В. Тер. архив. 1983; 10: 95-8. 7. Clemens JD, Horwitz RI, Jaffe CC. et al. N Engl J Med 1982; 307: 776-81. 8. Полежаев Л.В. Ахабадзе Л.В. Музлаева Н.А. Явич М.П. 1965 В кн. “Стимуляция регенерации мищцы сердца“ изд. “наука“. 9. Kim WH, Joo CU, Ku JH et ak. Cell cycle regulators during human atrial development. Korean J Intern Med 1998; 13 (2): 77 - 82. 10. Саркисов ДС. Регенерация и ее клиническое значение. М., Медицина, 1979. - 284 11. Kajstura J, Leri A, Finato N et al. Myocyte proliferation in endstage cardiac failure in humans. Proc Natl Acad Sci USA 1998; 95:8801 - 8805. 12. Проблемы трансплантологии и искусственных органов. Юбилейный сборник научных трудов НИИ ТиИО. М. 1994. - 142 13. Репин ВС. Трансплантация клеток: новые реальности в медицине. БЭБИМ 1998; 126 (приложение 1): 14 - 28. 14. В. П. Шахов, С. И. Попов, С. А. Афанасьев “Пластический потенциалмезенхимальних стволовых клеток костного мозга для лечения заболеваний связанных с повреждением сердечной ткани” журн. “кардиология” #2 2005. 45-46. 15. Репин ВС, Сухих ГТ. Медицинская клеточная биология. М., РАМН: БЭБИМ, 1998. - 200 с. 16. m. rogava 2001 “kardiomiopaTiis mqone avadmyofeSi mankieri wris klinikuri aspeqtebi” SromaTa krebuli II tomi, “Sinagani medicines miRwevebi da problemebi-2001” gv. 6-9. 17. Ю. Н. Беленков и соавт. 2003 “Мобилизация стволовых клеток костного мозга в лечении больных с сердечной недостаточностью”. 18. Reyes et al. (2002) J. Clin. Invest. 109: 337-346. 19. Yin AH, Miraglia S, Zanjani ED, et al. AC133, a novel marker for human hematopoietic stem and progenitor cells. Blood 1997; 90: 5002-12. 20. Miraglia S, Godfrey W, Yin AH, et al. A novel five-transmembrane hematopoietic stem cell antigen: Isolation, characterization and molecular cloning. Blood 1997; 90: 5013-21. 21. Bühring H-J, Seiffert M, Bock T et al. Expression of novel surface antigens on early hematopoietic cells. Ann NY Acad Sci 1999; 872: 25-39. 22. DeWynter EA, Buck D, Hart C, et al. CD34+AC133+ cells isolated from cord blood are highly enriched in long-term culture-initiating cells, NOD/SCID-repopulating cells and dendritic cell progenitors. Stem Cells1998; 16: 387-96. 23. Gehling UM, Ergün S, Schumacher U, et al. In vitro differentiation of endothelial cells from AC133-positive progenitor cells. Blood 2000; 95: 3106-12. 24. Peichev M, Naiyer AJ, Pereira D, et al. Expression of VEGFR-2 and AC133 by circulating human CD34+ cells identifies a population of functional endothelial precursors. Blood 2000; 95: 952-8. 25. Corbeil D, Roper K, Hellwig A, et al. The human AC133 hematopoietic stem cell antigen is also expressed in epithelial cells and targeted to plasma membrane protrusions. J Biol Chem 2000; 275: 5512-20. 26. Uchida et al. (2000) Proc. Natl. Acad. Sci.USA 97: 14720-14725. 27. Kaufman et al. (2001) Proc. Natl. Acad. Sci.USA 98: 10716-10721 28. Verfaillie et al. (2002) Nature 418: 41-49. 29. Kuci et al. (2003) MACS&more 7/1. 30. Peichev et al. (2000) Blood 95: 925-958. [931] 31. Gehling et al. (2000) Blood 95: 3106-3112. [943] 32. Stamm et al. (2003) Lancet 361: 45-46. 33. Piechazek et al. (2003) MACS&more 7/1. 34. Chasis, J., and N. Mohandas. 1992. Red blood cell glycophorins. Blood 80: 1869-1879 35. Chishti, A Y., J. Palek, D. FiSher. 1996. Reduced invasion and growth of Plasmodium falciparum into elliptocytic red blood cells with a combined deficiency of protein 4.1, glycophorin C, and p55. Blood 87; 3462-3469 36. Chien S: Red cell deformability and its relevance to blood flow. Annu Rev Physiol 37. Bruce, L. J., Ghosh, M. J. King. 2002. Absence of CD47 in protein 4.2-deficient hereditary spherocytosis in man: an interaction between the Rh complex and the band 3 complex. Blood 100: 1878-1885 38. Hassoun, H., T. Hanada. 1998. Complete deficiency of glycophorin A in red blood cells from mice with targeted inactivation of the band 3 (AE1) gene. blood 91:2146-2151. 39. “модeлировaниe пeптидов и Белков в мeмбрaнном окружeнии. II. структурныe и энeргeтичeскиe Аспeкты гликофоринa А в Бислоe” П. Е. Волынский, Д. Е. Нольде, А. С. Арсеньев, Р. Г. Ефремов. биологическая химия 2000 №3 с 163-172 40. Mohandas N, Phillips WM, Bessis M: Red blood cell deformability and hemolytic anemias. Semin Hematol 16:95, 1979 |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||